题目内容
【题目】某学习小组测定某硫酸厂的度水(含有H2SO4、HCl,不含固体杂质)中H2SO4的含量。取100g废水于烧杯中,加入100g BaCl2溶液,恰好完全反应,反应过程如图所示。(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
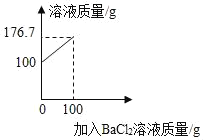
(1)充分反应后生成沉淀的质量为_____g;
(2)求该工业废水中硫酸的质量分数。_____(计算结果精确到0.1%)
【答案】23.3 9.8%
【解析】
(1)由质量守恒定律可知生成的硫酸钡的质量为:100g+100g﹣176.7g=23.3g
(2)设100g该工业废水中硫酸的质量位x。
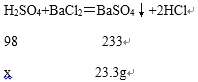
![]()
解得:x=9.8g
该工业度水中硫酸的质量分数为:![]() =9.8%
=9.8%
故答案为:(1)23.3;(2)该工业度水中硫酸的质量分数为9.8%;

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
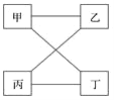
【题目】如表提供的四组物质符合图示,相连物质间在一定条件下可以发生反应的是( )
甲 | 乙 | 丙 | 丁 | |
A | CO | O2 | H2SO4 | CuO |
B | Mg | HCl | CuSO4 | NaOH |
C | KOH | SO3 | NaOH | CuSO4 |
D | Na2CO3 | Ca(OH)2 | HCl | CaCl2 |
A. A
B. B
C. C
D. D
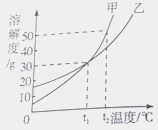
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
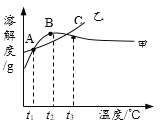
A. 甲为NH4Cl
B. t3℃应介于30℃~40℃
C. 乙物质的饱和溶液从t2升温到t3,溶液的溶质质量分数不变
D. 甲、乙饱和溶液从t3降温到t1,析出晶体(均不带结晶水)的质量一定相等