题目内容
燃烧是生活中常常见到的现象,氧气具有支持燃烧的性质.(提示:假设蜡烛中不含氧元素)
(1)上述三个实验的共同点是______(填序号);
①都有光或火焰产生 ②都放热 ③生成物都为固体
④都是化合反应 ⑤都是氧化反应 ⑥生成物都是氧化物
(2)硫燃烧实验中水的作用是______;
(3)铁丝燃烧的化学反应式为______ Fe3O4
【答案】分析:(1)根据燃烧的现象和反应物、生成物的种类考虑;(2)根据二氧化硫的有毒性考虑;(3)根据方程式的写法考虑;(4)根据化合价的变化判断其氧化性;根据实验现象考虑能否支持燃烧,根据质量守恒定律推测所含成分和元素,根据方程式的写法写出正确的方程式.
解答:解:(1)硫燃烧发出蓝紫色火焰放出热量,生成物是气体,反应属于化合反应,蜡烛燃烧生成物是气体和液体不属于化合反应、铁丝燃烧生成物是固体,属于化合反应,都放出光,放出热量,都有氧气参加,都属于氧化反应,生成物二氧化硫、二氧化碳、水、四氧化三铁都属于氧化物;
(2)硫燃烧产物是二氧化硫,属于有毒气体污染空气,用水来吸收二氧化硫,防止污染空气;
(3)反应物是铁和氧气,生成物是四氧化三铁,用观察法配平即可,反应条件是点燃;
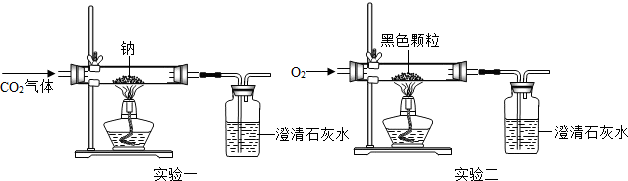
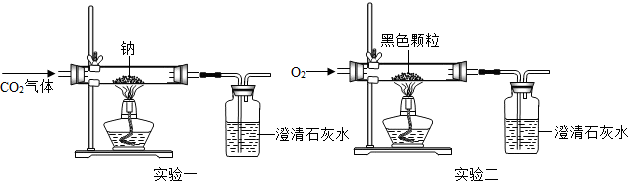
(4)氧元素从O价变为-2价,化合价降低体现了氧化性;通过钠在二氧化碳中燃烧,说明二氧化碳能支持燃烧;由于反应物中含有碳元素,所以生成物中的黑色物质是碳;碳燃烧的反应物是碳和氧气,生成物是二氧化碳,反应条件是点燃;根据质量守恒定律可知反应前后元素种类不变,氢氧化钠中含有氢元素,反应物中没有氢元素,所以不可能是氢氧化钠;钠与二氧化碳反应的反应物是钠和二氧化碳,生成物是碳酸钠和碳,反应条件是点燃,用观察法配平即可.
故答案为:(1)①②⑤⑥
(2)吸收有毒的SO2
(3)3Fe+2O2 Fe3O4
Fe3O4
(4)氧元素从O价变为-2价
(得出结论) 能(猜想与假设)C(得出结论)C+O2 CO2(猜想与假设)ⅡNa与CO2中不含氢元素
CO2(猜想与假设)ⅡNa与CO2中不含氢元素
(得出结论)4Na+3CO2 2Na2CO3+C
2Na2CO3+C
点评:同归回答本题知道了物质燃烧时共同点的寻找方法,根据质量守恒定律来分析问题的方法,进一步熟悉了方程式的书写方法.
解答:解:(1)硫燃烧发出蓝紫色火焰放出热量,生成物是气体,反应属于化合反应,蜡烛燃烧生成物是气体和液体不属于化合反应、铁丝燃烧生成物是固体,属于化合反应,都放出光,放出热量,都有氧气参加,都属于氧化反应,生成物二氧化硫、二氧化碳、水、四氧化三铁都属于氧化物;
(2)硫燃烧产物是二氧化硫,属于有毒气体污染空气,用水来吸收二氧化硫,防止污染空气;
(3)反应物是铁和氧气,生成物是四氧化三铁,用观察法配平即可,反应条件是点燃;
(4)氧元素从O价变为-2价,化合价降低体现了氧化性;通过钠在二氧化碳中燃烧,说明二氧化碳能支持燃烧;由于反应物中含有碳元素,所以生成物中的黑色物质是碳;碳燃烧的反应物是碳和氧气,生成物是二氧化碳,反应条件是点燃;根据质量守恒定律可知反应前后元素种类不变,氢氧化钠中含有氢元素,反应物中没有氢元素,所以不可能是氢氧化钠;钠与二氧化碳反应的反应物是钠和二氧化碳,生成物是碳酸钠和碳,反应条件是点燃,用观察法配平即可.
故答案为:(1)①②⑤⑥
(2)吸收有毒的SO2
(3)3Fe+2O2
 Fe3O4
Fe3O4(4)氧元素从O价变为-2价
(得出结论) 能(猜想与假设)C(得出结论)C+O2
 CO2(猜想与假设)ⅡNa与CO2中不含氢元素
CO2(猜想与假设)ⅡNa与CO2中不含氢元素(得出结论)4Na+3CO2
 2Na2CO3+C
2Na2CO3+C点评:同归回答本题知道了物质燃烧时共同点的寻找方法,根据质量守恒定律来分析问题的方法,进一步熟悉了方程式的书写方法.

练习册系列答案
相关题目