题目内容
(2013?金台区一模)铜锌合金是铜和锌的合金,具有优异的机械性能.可以用来制造机器零件及日常用品.为了测定某块铜锌合金中的铜锌的质量分数.某课外化学小组做了如下实验:准确量取这种合金9克,加入足量稀盐酸中,充分反应,产生的气体质量为0.2克.试计算合金中铜的质量分数.
分析:根据黄铜的成分铜和锌的性质可知,加入稀盐酸时,只有锌与稀盐酸反应生成了氯化锌和氢气;由生成氢气的质量,根据反应的化学方程式列式计算出参加反应锌的质量,进而计算出铜的质量和铜的质量分数.
解答:解:设合金中锌的质量为x.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
=
x=6.5g
合金中铜的质量分数为
×100%≈27.8%.
答:合金中铜的质量分数为27.8%.
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| 2 |
| x |
| 0.2g |
合金中铜的质量分数为
| 9g-6.5g |
| 9g |
答:合金中铜的质量分数为27.8%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目

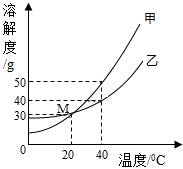 (2013?金台区一模)甲、乙两种固体的溶解度曲线如右图所示.下列说法中,不正确的是( )
(2013?金台区一模)甲、乙两种固体的溶解度曲线如右图所示.下列说法中,不正确的是( )