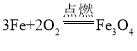题目内容
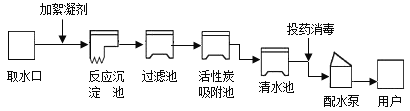
【题目】科学方法对化学学习起着事半功倍的作用。下图是某同学整理的铁及其化合物知识网络图。
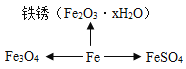
(1)分类归纳是研究化学物质的重要方法。
①铁丝燃烧生成Fe3O4的过程中___(选填”放出”或“吸收”)热量。
②铁制品的锈蚀过程,实际上是铁与空气中的___等发生化学反应的过程。
③与FeSO4中铁元素化合价相同的铁氧化物的化学式是____。
(2)控制变量、设计对比实验是实验探究的重要方法。
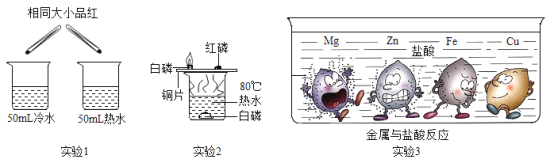
①实验l中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短。这是因为___。
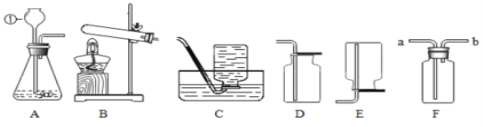
②实验2中使用铜片是为了对比___不同。
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论不正确的是___。(填字母)
a铜不能发生置换反应
b四种金属中金属活动性最强的是Mg
c等质量的锌和铁分别与足量的盐酸反应生成气体质量:Zn比Fe多
【答案】放出 氧气和水 FeO 温度越高,分子运动越剧烈 可燃物的着火点 ac
【解析】
铁和氧气在点燃的条件下生成四氧化三铁,放出大量的热,铁制品的锈蚀过程,实际上是铁与空气中的氧气和水等发生化学反应;根据化合价代数和为零,物质的化学性质与原子的最外层电子数有关。
(1)①铁和氧气在点燃的条件下生成四氧化三铁,放出大量的热,故铁丝燃烧生成Fe3O4的过程中放出热量。
②铁制品的锈蚀过程,实际上是铁与空气中的氧气和水等发生化学反应的过程。
③在FeSO4中硫酸根离子显示2价,亚铁离子显示+2价,故与铁元素化合价相同的铁的氧化物是氧化亚铁,化学式是FeO。
(2)①实验l中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短。这是因为温度越高,分子运动越剧烈。
②白磷的着火点低,先燃烧,红磷的着火点高,后燃烧,故实验2中使用铜片是为了对比可燃物的着火点不同。
③a、铜不能与酸发生反应,铜可以将硝酸银中的银置换出来,不能说铜不会发生置换反应,故a不正确;
b、镁表面的气泡产生最剧烈,四种金属中金属活动性最强的是Mg,故b正确;
c、每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe少,故c不正确。故选ac。

【题目】某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质不溶于水,不与稀盐酸反应)。根据实验数据计算:
实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 20 | 15 |
2 | 20 | 10 |
3 | 20 | 6.8 |
4 | 20 | 6.8 |
(1)四次实验中,第________次石灰石中碳酸钙有剩余,第____次实验中盐酸有剩余。
(2)样品中碳酸钙的质量分数是________。
(3)20g这种样品与足量稀盐酸反应后可产生二氧化碳的质量是多少________?(精确到0.1g)