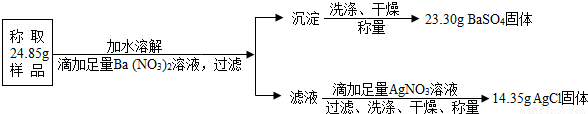
题目内容
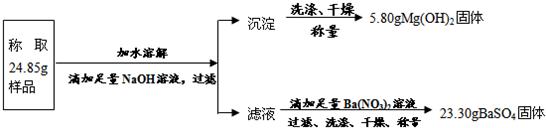
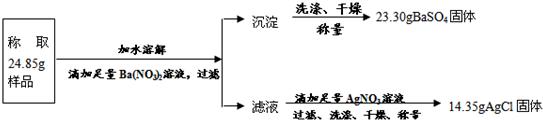
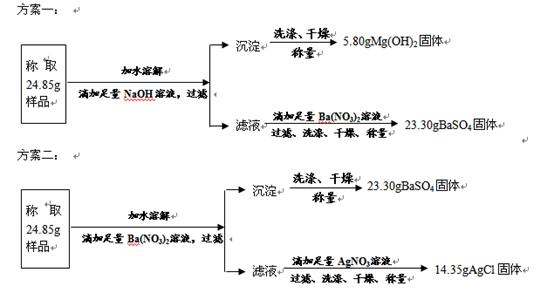
“钾泻盐”的化学式为MgSO4·KCl·xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与MgSO4的混合溶液.某化学活动小组设计了如下种实验方案:
以下说法不正确的是(相对分子量:MgSO4-120 BaSO4-233 AgCl-143.5 KCl-74.5)
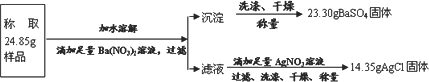
A.该方案能够计算出“钾泻盐”中KCl的质量分数
B.足量Ba(NO3)2溶液是为了与MgSO4充分反应
C.“钾泻盐”化学式中x=2
D.上述实验数据的测定利用学校实验室里的托盘天平即可完成
答案:CD

练习册系列答案
相关题目