题目内容
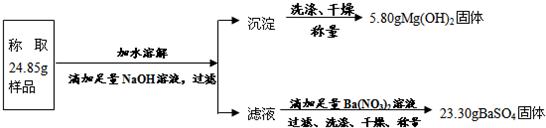
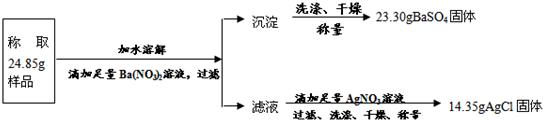
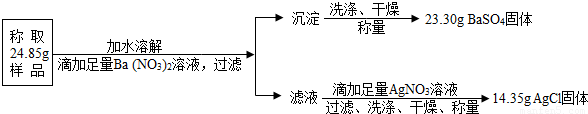
“钾泻盐”的化学式为 MgSO4?KCl?xH2O 是一种制取钾肥的重要原料,它溶于水得 KCl与 MgSO4的混合溶液.两个化学小组对某“钾泻盐”样品进行了有关探究.
(1)甲组为了检验该“钾泻盐”样品的水溶液中含有SO42-、Cl- 应使用的试剂是
(2)乙组为了测定“钾泻盐”中KCl的质量分数,设计了如下三个方案:
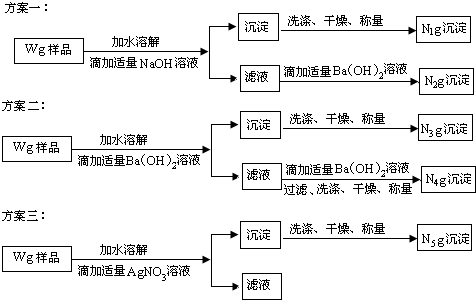
①方案一中涉及的化学方程式有
②方案二中,滴加适量 Ba(OH)2 溶液的作用是
③要测得样品中 KCl的质量分数,你认为方案
④若用方案三测样品中KCl的质量分数,测得结果偏
⑤选择合理方案中的数据写出样品中 KCl 的质量分数的表达式 (可能用到的 相对分子质量:KCl-74.5Mg(OH)2-58BaSO4-233AgCl-143.5MgSO4-120).
(1)甲组为了检验该“钾泻盐”样品的水溶液中含有SO42-、Cl- 应使用的试剂是
Ba(NO3)2、AgNO3
Ba(NO3)2、AgNO3
(填化学式)溶液和稀硝酸. (2)乙组为了测定“钾泻盐”中KCl的质量分数,设计了如下三个方案:

①方案一中涉及的化学方程式有
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓;Na2SO4+Ba(OH)2═BaSO4↓+2NaOH
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓;Na2SO4+Ba(OH)2═BaSO4↓+2NaOH
.②方案二中,滴加适量 Ba(OH)2 溶液的作用是
除去MgSO4
除去MgSO4
.③要测得样品中 KCl的质量分数,你认为方案
二
二
比较合理(填“一”或“二”),另一个不合理的理由是无法测定KCl的质量
无法测定KCl的质量
.④若用方案三测样品中KCl的质量分数,测得结果偏
高
高
(填“高”、“低”或“无 影响”).⑤选择合理方案中的数据写出样品中 KCl 的质量分数的表达式 (可能用到的 相对分子质量:KCl-74.5Mg(OH)2-58BaSO4-233AgCl-143.5MgSO4-120).
分析:(1)根据SO42-、Cl-的检验方法或者复分解反应的条件即可.
(2)①根据复分解反应的条件---沉淀即可.
②根据过滤的特点,沉淀最后残留在滤纸上,谁生成沉淀,谁就被除去.
③列出方程式并结合已知条件即可判断那种方法可以测出KCl的质量分数.
④沉淀包含两种:硫酸银和氯化银,因此结果会偏高.
⑤列出化学方程式即可算出.
(2)①根据复分解反应的条件---沉淀即可.
②根据过滤的特点,沉淀最后残留在滤纸上,谁生成沉淀,谁就被除去.
③列出方程式并结合已知条件即可判断那种方法可以测出KCl的质量分数.
④沉淀包含两种:硫酸银和氯化银,因此结果会偏高.
⑤列出化学方程式即可算出.
解答:解:(1)检验物质一般要求反应现象明显,SO42-和Ba(NO3)2,Cl-和AgNO3都有沉淀生成,故答案为:Ba(NO3)2、AgNO3.
(2)①书写化学方程式注意反应条件和沉淀符号,故答案为:2NaOH+MgSO4═Na2SO4+Mg(OH)2↓;
Na2SO4+Ba(OH)2═BaSO4↓+2NaOH.
②Ba(OH)2和MgSO4反应生成硫酸钡沉淀和氢氧化镁沉淀,因此可以出去MgSO4,故答案为:除去MgSO4.
③方案二中,KCl和AgNO3生成AgCl沉淀,并且AgCl沉淀的质量已经给出,所以可以计算出KCl的质量和质量分数,故答案为:二,无法测定KCl的质量.
④沉淀包含两种:硫酸银和氯化银,因此结果会偏高.故答案为:高.
⑤设KCl的质量为X,
KCl+AgNO3═AgCl↓+KNO3
74.5 143.5
x N4
═
得X═
所以KCl的质量分数是:
×100%
答:KCl的质量分数是
×100%.
(2)①书写化学方程式注意反应条件和沉淀符号,故答案为:2NaOH+MgSO4═Na2SO4+Mg(OH)2↓;
Na2SO4+Ba(OH)2═BaSO4↓+2NaOH.
②Ba(OH)2和MgSO4反应生成硫酸钡沉淀和氢氧化镁沉淀,因此可以出去MgSO4,故答案为:除去MgSO4.
③方案二中,KCl和AgNO3生成AgCl沉淀,并且AgCl沉淀的质量已经给出,所以可以计算出KCl的质量和质量分数,故答案为:二,无法测定KCl的质量.
④沉淀包含两种:硫酸银和氯化银,因此结果会偏高.故答案为:高.
⑤设KCl的质量为X,
KCl+AgNO3═AgCl↓+KNO3
74.5 143.5
x N4
| X |
| N4 |
| 74.5 |
| 143.5 |
得X═
| 74.5N4 |
| 143.5 |
所以KCl的质量分数是:
| 74.5N4 |
| 143.5W |
答:KCl的质量分数是
| 74.5N4 |
| 143.5W |
点评:本题主要是考查学生对复分解反应的条件的理解能力,同时注意化学方程式的书写规范.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目