题目内容
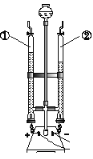
【题目】下面图示是硫粉、红磷、光亮的细铁丝在氧气中燃烧的实验装置:
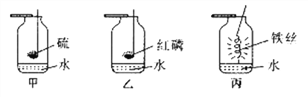
(1)三个实验有一些共同的特点:在反应条件方面,三个实验都要________,在能量变化方面,三个实验都是________(填“吸热”或“放热”),在反应的基本类型方面,三个反应都是___________反应。
(2)甲中产生_______色的火焰,反应的文字表达式是__________________________。
(3)乙中产生浓厚的白______,反应的文字表达式是___________________________。
(4)丙中的反应现象是铁丝剧烈燃烧,____________,生成_____色固体。
(5)三个集气瓶里都放有少量的水,其中甲中水的目的是_______________________。
【答案】 点燃 放热 化合 蓝紫 硫 + 氧气 ![]() 二氧化硫 烟 磷 + 氧气
二氧化硫 烟 磷 + 氧气 ![]() 五氧化二磷 火星四射 黑 吸收二氧化硫,防止污染空气
五氧化二磷 火星四射 黑 吸收二氧化硫,防止污染空气
【解析】(1)三个实验反应条件都是点燃,在能量变化方面,三个实验都是燃烧,都是放热的,三个反应都符合“多变一”的特点,都属于化合反应;
(2)硫在氧气中燃烧发出蓝紫色火焰,生成具有刺激性气味的气体(二氧化硫),反应的文字表达式是硫 + 氧气 ![]() 二氧化硫;
二氧化硫;
(3)磷在氧气中燃烧产生浓厚的白烟(五氧化二磷),反应的文字表达式是磷 + 氧气 ![]() 五氧化二磷;
五氧化二磷;
(4)铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体(四氧化三铁);
(5)硫在氧气中燃烧生成二氧化硫,集气瓶里都放有少量的水,吸收二氧化硫,防止污染空气。

练习册系列答案
相关题目