题目内容
【题目】硫酸是重要的化工原料,可用于生产化肥农药火药等,硫酸生产厂产生的烟气中含有SO2气体,直接排放会形成酸雨,如图是某硫酸厂除去烟气中SO2的流程图,回答下列问题:
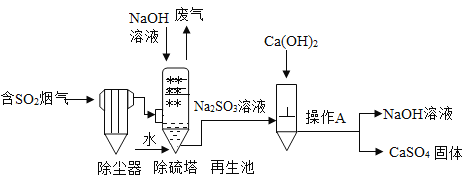
(1)除硫塔内,将NaOH溶液呈雾状向下喷洒,其目的是________;SO2发生反应的化学方程式是________(写一个)。
(2)再生池内加入的氢氧化钙也可用________代替。
(3)图中操作A指的是________,流程中可以循环利用的物质是________。
【答案】增大接触面积,使吸收更充分 ![]() 氧化钙 过滤 NaOH
氧化钙 过滤 NaOH
【解析】
(1)将NaOH溶液呈雾状向下喷洒,目的是使氢氧化钠溶液与二氧化硫气体充分接触,更有利于吸收二氧化硫气体;氢氧化钠吸收SO2并与二氧化硫发生反应,化学方程式是![]() 。
。
(2)再生池内加入的氢氧化钙目的是使亚硫酸钠转化为氢氧化钠和亚硫酸钙,氢氧化钙也可用氧化钙代替,因为氧化钙与水生成氢氧化钙。
(3)通过操作A可以使亚硫酸钙固体与氢氧化钠溶液分离,所以操作A应该是过滤。通过操作A得到氢氧化钠溶液,可以用于除硫塔中除二氧化硫气体,所以该流程中可以循环利用的物质是氢氧化钠。

【题目】有一包白色固体,可能含有NaOH、Na2CO3、Na2SO4 、NaCl、 Ba(NO3)2中的一种或几种,为探究其组成,某学习小组设计方案并进行了如下实验:
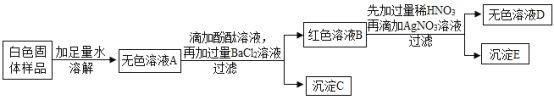
(1)上述实验中,过滤操作用到的玻璃仪器有漏斗、烧杯和______________。
(2)小李同学通过上述实验推知:自色固体样品中一定不含有______________。
(3)为确定白色固体样品中可能存在的物质,小强对沉淀C进行实验。
实验操作 | 现象 | 结论及化学方程式 |
取少量沉淀C于试管中,加入足量稀盐酸 | 有气泡产生,沉淀部分消失 | 白色固体样品中一定含有__________。 该反应的化学方程式为:___________。 |
(4)小明同学认为白色固体中还有物质不能确认其是否存在,其理由是:______________,如要确认,只需将上述实验方案中所加的一种试剂改为______________即可。
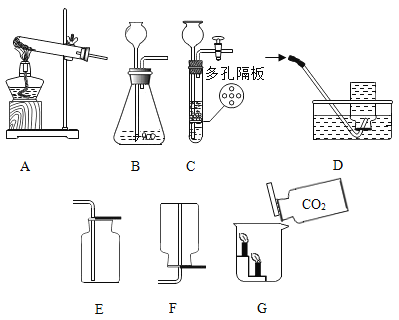
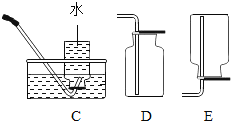
【题目】(1)根据下图的实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
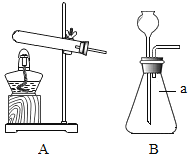
①图B中仪器a的名称_____。
②实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为:_____,发生和收集装置为_____(填字母)。
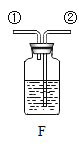
③实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的_____端口(填“①”或“②”)通入,F中发生的化学方程式为_____。
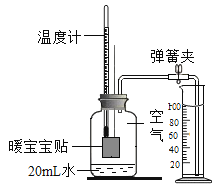
(2)为了探究碱的性质,进行如图所示的实验。

①图甲所示,加入一定量的盐酸后,溶液由红色变为了无色,证明了盐酸和NaOH发生了中和反应,且反应后的溶液中一定没有的溶质是_____。张明对甲实验所得溶液的溶质成分产生了兴趣,对反应后溶液变为无色提出了以下两种猜想:
猜想1:溶质成分只有NaCl;
猜想2:溶质成分为_____。
(进行实验)为了验证自己的猜想正确,张明进行了如下实验,请你和他一起完成下列实验报告:
实验操作 | 实验现象 | 实验结论 |
取少量甲实验所得溶液于试管中,并往试管中加入_____ | 观察到_____ | 猜想2正确 |
②如图乙和丙所示,同时将两支充满CO2的相同试管分别倒扣在等体积的水和NaOH溶液中,一段时间后丙中试管内液面高于乙。说明NaOH与CO2发生了反应,该反应的化学方程式为_____。本实验中乙的作用是_____。