题目内容
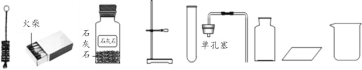
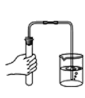
【题目】已知:![]() ,为探究铜和浓硫酸的反应及生成的二氧化硫气体的部分性质,某同学设计如图实验(图中脱脂棉团蘸有紫色石蕊溶液)。下列关于该实验的说法错误的是( )
,为探究铜和浓硫酸的反应及生成的二氧化硫气体的部分性质,某同学设计如图实验(图中脱脂棉团蘸有紫色石蕊溶液)。下列关于该实验的说法错误的是( )

A. 该装置便于控制铜和浓硫酸反应的发生和停止
B. 铜丝绕成螺旋状是为了加快铜和浓硫酸的反应
C. 实验中可观察到脱脂棉团变红
D. 氢氧化钠溶液用于吸收尾气SO2,其反应的基本类型是复分解反应
【答案】D
【解析】
A. 该装置可通过上下移动粗铜丝控制铜和浓硫酸反应的发生和停止,此选项正确;
B. 铜丝绕成螺旋状是为了增大反应物的接触面积,加快铜和浓硫酸的反应,此选项正确;
C. 实验中生成的二氧化硫与紫色石蕊溶液中的水反应生成酸,生成的酸使紫色石蕊溶液变红,可观察到脱脂棉团变红,此选项正确;
D. 氢氧化钠溶液用于吸收尾气SO2,2NaOH+SO2 =Na2SO3 +H2O,由两种化合物互相交换成分生成另外两种化合物的反应是复分解反应,该反应不是复分解反应,此选项错误。
故选D。

练习册系列答案
相关题目
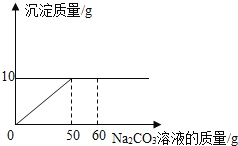
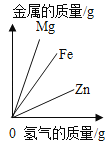
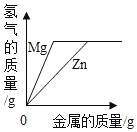
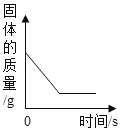
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
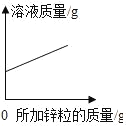
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D
【题目】煅烧石灰石(主要成分 CaCO3)生成生石灰(CaO)和二氧化碳。为了测定某石灰石中碳酸钙(CaCO3)的含量,现称取 24.0g 石灰石样品,进行四次高温煅烧、冷却,称量剩余固体的质量 (杂质不参加反应),记录实验数据如下:
操作 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 21.6g | 19.2g | 15.2g | 15.2g |
试计算:
(1)完全反应后生成二氧化碳的质量为_____;
(2)求该石灰石样品中碳酸钙的质量_____。