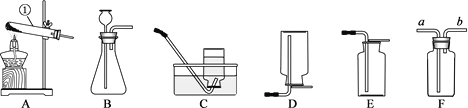
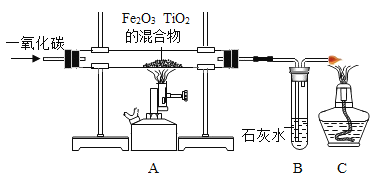
题目内容
【题目】今年国庆假期,小文从梧桐山带回一瓶浑浊的山泉水,他想模拟自来水厂的净水过程,制成自来水,其实验过程如图所示,请回答以下问题。
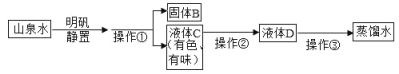
(1)操作①需要用到的玻璃仪器除了漏斗和烧杯,还有_______;得到的液体C属于___ (填 “纯净物”或“混合物”),因为_________。若经过操作①后,所得液体C中仍有浑浊,原因可能是_______(可多选)。
a.漏斗内的滤纸有破损 b.漏斗下端未靠在烧杯内壁 c.漏斗内液面高于滤纸的边缘
(2)操作②过程中常用活性炭来除去一些异味和色素,这是利用活性炭的________作用。
(3)小文想知道经净化后得到的液体D属于软水还是硬水,他可以用_____ 进行区分:生活中常用_____方法降低水的硬度。
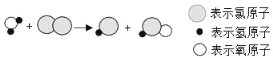
(4)操作③是对水的消毒杀菌,目前有些自来水厂用氯气进行消毒,消毒过程中会发生如图所示化学反应,其反应的微观过程如图所示,写出如图所示的化学方程式 _____。
(5)若想进一步将液体D变成纯净水,可以通过_____ 操作来实现。
【答案】玻璃棒 混合物 液体C中仍含有一些可溶性的杂质 ac 吸附 肥皂水 煮沸 H2O +Cl2==HCl+HClO 蒸馏
【解析】
(1)操作①是过滤,过滤中需要用到的玻璃仪器除了漏斗和烧杯,还有玻璃棒;得到的液体C中仍含有一些可溶性的杂质,所以液体C属于混合物。若经过滤操作后,所得液体C中仍有浑浊,可能是漏斗内的滤纸有破损,起不到过滤作用,还可能是漏斗内液面高于滤纸的边缘,高于液面的液体直接从滤纸与漏斗之间的空隙流下,而使液体C浑浊,故选ac。
(2)活性炭具有吸附作用,能除去异味和色素。
(3)区分软水、硬水用肥皂水:生活中常用煮沸的方法降低水的硬度。
(4)根据反应的微观过程示意图可知,反应的化学方程式为:H2O +Cl2==HCl+HClO
(5)蒸馏后得到的液体是纯净水。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案