题目内容
【题目】(1)写出下列化学符号:
①3个氯离子______②标出五氧化二磷中磷元素的化合价_____③硫酸溶液中的溶质_______
(2)将空格里要画出的微观示意图填在横线上:

____________________________、_____________________________________
【答案】3Cl- ![]() H2SO4
H2SO4 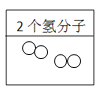
【解析】
(1)①由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;若表示多个该离子,就在其元素符号前加上相应的数字,故3个氯离子可表示为:3Cl-;
②五氧化二磷中氧元素显-2价,磷元素显+5价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故五氧化二磷中磷元素的化合价可表示为:![]() ;
;
③硫酸溶液中的溶质硫酸,其化学式为H2SO4;
(2每个氢分子由两个氢原子构成,故填两个氢分子,如图: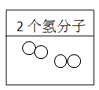 ;填入两个独立的氧原子,如图:
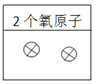
;填入两个独立的氧原子,如图: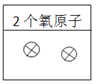 。
。

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】兴趣小组的同学对铝的相关知识进行探究。
(知识回顾)
(1)铝是地壳中含量最多的金属元素,在自然界主要以化合态的形式存在于氧化铝中。下列说法不正确的是 _____。
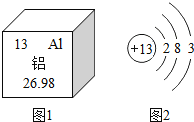
A 铝原子的中子数为13
B 铝离子核外有三个电子层
C 化合物中铝元素通常显+3价
D 铝可作导线是由于它具有良好的导电性
(铝的冶炼)
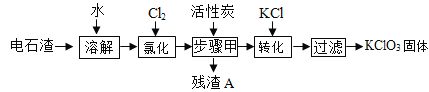
工业上常用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝,工艺流程如图。氧化铝是两性氧化物,与酸、碱都能发生反应,Al2O3+2NaOH=2NaAlO2+H2O。请回答以下问题:
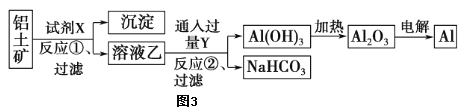
(2)试剂X是_________选填氢氧化钠溶液或盐酸)。
(3)反应①后过滤所得的沉淀是___________。
(4)写出反应②的化学方程式___________________。
(定性研究)
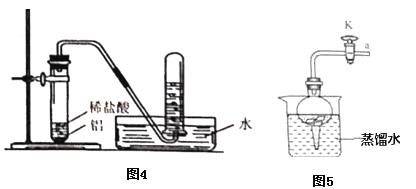
(提出问题)如图所示装置中铝和稀盐酸反应可以制取氢气,那么铝能否与水反应生成氢气呢?
(查阅资料)
物质 | 钠与水 | 铝与水 | 汞与水 |
能否发生反应 | 能反应 | 能反应 | 不反应 |
(交流与讨论)
(5)铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,起到保护膜的作用。如生活中可用铝壶烧水。铝与氧气反应的化学方程式为_____________。
(6)除去铝表面氧化铝薄膜的方法有(举一例)_______。除上述方法外,还可以将铝片浸入氯化汞( HgCl2)溶液中,形成铝汞齐(铝汞合金)破坏铝表面致密的氧化膜且防止其重新生成。
(实验探究)
(7)将铝片完全浸入氯化汞(HgCl2)溶液中1分钟左右,取出,立即用流水冲洗干净后加入到蒸馏水中(如图),其表面生成大量气泡、周围出现白色沉淀。若关闭导管上的活塞K,反应停止,其原理是_____________。
(8)在导管口a处涂肥皂水,发现导管口有气泡形成,当气泡离开导管后,气泡______(填“下沉”或“上升”),用燃着的木条点燃气泡,发出爆鸣声。
(实验结论)
(9)铝能与水反应生成氢气。写出铝与水反应生成氢氧化铝和氢气的化学方程式____________。
(定量研究)兴趣小组取8g铝镁合金样品,将30g氢氧化钠溶液平均分成三份依次加入样品中(镁与氢氧化钠溶液不反应,铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
剩余固体的质量/g | 5.3 | 2.6 | 2.0 |
(10)该合金中,镁与铝的质量比为 _____。
(11)所用氢氧化钠溶液中溶质的质量分数为多少?(写出计算过程)____