题目内容
【题目】水是及其宝贵的自然资源,在生产生活中有着及其广泛的应用。
(一)自然界的水
(1)从物质变化及分子角度看,自然界的水循环主要是由_____的运动引起的。
(二)生活中的水
(2)自来水生产过程常加入活性炭,作用是_____,该过程是_____变化(填“物理”或“化学”)。
(3)生活中鉴别硬水、软水的方法是:取少量水样,加入_____,并搅拌,出现大量浮渣现象的为_____。生活常用_____的方法对硬水进行软化。
(4)保护水资源是我们义不容辞的责任。下列做法不合理的是_____(填字母)。
A 严格监管化肥和农药的使用 B 不间断地放水洗衣服
C 积极探索污水处理的新技术 D 抑制水中所有动、植物的生长
(三)探究水的组成
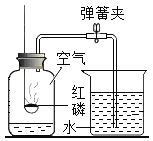
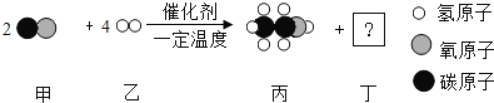
(5)“氢气燃烧”是人们认识水组成的开始氢气在空气中燃烧,在其火焰上方罩一只干冷的烧杯,可观察到_____。
已知:同温同压下,体积相同的任何气体具有相同的分子数。欲使1L氢气完全燃烧,所需空气的体积至少约为_____L。
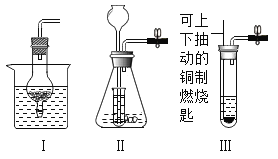
(6)“电解法”证明水的组成(装置如图1所示,电极不与水及生成的气体反应)
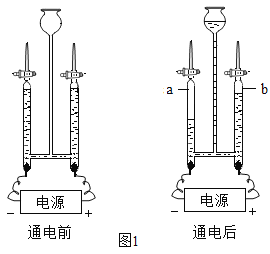
①该实验使用的是低压_____电(填“直流”或“交流”);
②气体b 为_____;
③通电时反应的化学方程式为_____;
④通电后中间长颈漏斗内液面上升的原因是_____。
⑤下列关于电解水的说法中正确的是_____(填字母)。
A 水分子发生了改变
B 氢原子和氧原子没有发生变化
C 水分子是该变化中的最小微粒
【答案】水分子 吸附水中的色素和异味 物理 肥皂水 硬水 煮沸 BD 干冷烧杯内壁有水雾(小水珠、变模糊) 2.5L 直流 O2(或氧气) 2H2O![]() 2H2↑+O2↑ a、b两管内汇聚气体,气压变大,将水压入中间容器内 AB
2H2↑+O2↑ a、b两管内汇聚气体,气压变大,将水压入中间容器内 AB
【解析】
电解水正极生成氧气,负极生成氢气。
(1)水是由水分子构成的,从物质变化及分子角度看,自然界的水循环主要是由水分子的运动引起的。
(2)自来水生产过程常加入活性炭,具有吸附性,作用是吸附水中的色素和异味,该过程没有新物质生成,是物理变化。
(3)鉴别硬水、软水是加肥皂水,产生泡沫较多,浮渣较少的为软水,产生泡沫较少,浮渣较多的为硬水,生活中鉴别硬水、软水的方法是:取少量水样,加入肥皂水,并搅拌,出现大量浮渣现象的为硬水。生活常用煮沸的方法对硬水进行软化。
(4)A、严格监管化肥和农药的使用,可以保护水资源,故A正确;
B、不间断地放水洗衣服,会浪费水资源,故B不正确;
C、积极探索污水处理的新技术,可以保护水资源,故C正确;
D、抑制水中所有动、植物的生长,不利于保护水资源,故D不正确。故选BD。
(5)氢气在氧气中点燃生成水,“氢气燃烧”是人们认识水组成的开始氢气在空气中燃烧,在其火焰上方罩一只干冷的烧杯,可观察到干冷烧杯内壁有水雾(小水珠、变模糊)。
欲使1L氢气完全燃烧,需要0.5L氧气,所需空气的体积至少约为![]() 。
。
(6)①该实验使用的是低压直流电。
②电解水正极生成氧气,负极生成氢气,故气体b 和电源正极相连,为O2(或氧气)。
③电解水生成氢气和氧气,通电时反应的化学方程式为2H2O![]() 2H2↑+O2↑。
2H2↑+O2↑。
④通电后中间长颈漏斗内液面上升的原因是a、b两管内汇聚气体,气压变大,将水压入中间容器内。
⑤A、电解水生成氢气和氧气,水分子发生了改变,故A正确;
B、化学变化是分子的破裂,原子的重新组合,氢原子和氧原子没有发生变化,故B正确;
C、分子是保持化学性质的最小微粒,原子是化学变化中的最小微粒,氢原子和氧原子是该变化中的最小微粒,故C不正确。故选AB。