题目内容
有一碳酸钠溶液,质量为100克,向其中倒入200克稀硫酸,恰好完全反应,得溶液291.2克,求:
(1)碳酸钠溶液中溶质的质量分数;
(2)所得溶液中溶质的质量分数.
(1)碳酸钠溶液中溶质的质量分数;
(2)所得溶液中溶质的质量分数.
生成二氧化碳的质量为100g+200g-291.2g=8.8g
设碳酸钠的质量为x,生成硫酸钠的质量为y
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 8.8g
=
x=21.2g
=
y=28.4g
(1)碳酸钠溶液中溶质的质量分数为
×100%=21.2%
(2)反应后所得溶液的溶质质量分数=
×100%=9.75%
答:(1)碳酸钠溶液中溶质的质量分数为21.2%
(2)反应后所得溶液的溶质质量分数为9.75%
故答案为:(1)21.2% (2)9.75%
设碳酸钠的质量为x,生成硫酸钠的质量为y
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 8.8g
| 106 |
| 44 |
| x |
| 8.8g |
| 142 |
| 44 |
| y |
| 8.8g |
(1)碳酸钠溶液中溶质的质量分数为
| 21.2g |
| 100g |
(2)反应后所得溶液的溶质质量分数=
| 28.4g |
| 291.2g |
答:(1)碳酸钠溶液中溶质的质量分数为21.2%
(2)反应后所得溶液的溶质质量分数为9.75%
故答案为:(1)21.2% (2)9.75%

练习册系列答案
相关题目
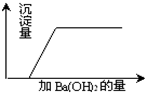 37、有一混合溶液是由硝酸、碳酸钠、硫酸、氯化铜四种物质中的两种混合而成,向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入 Ba(OH)2溶液体积的关系如图所示,据此回答:
37、有一混合溶液是由硝酸、碳酸钠、硫酸、氯化铜四种物质中的两种混合而成,向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入 Ba(OH)2溶液体积的关系如图所示,据此回答: