题目内容
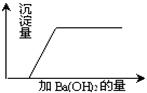
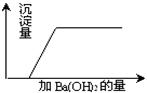
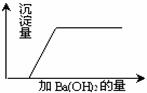
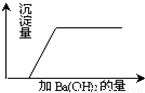
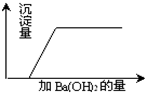 37、有一混合溶液是由硝酸、碳酸钠、硫酸、氯化铜四种物质中的两种混合而成,向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入 Ba(OH)2溶液体积的关系如图所示,据此回答:
37、有一混合溶液是由硝酸、碳酸钠、硫酸、氯化铜四种物质中的两种混合而成,向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入 Ba(OH)2溶液体积的关系如图所示,据此回答:(1)该混合溶液是由
HNO3
和CuCl2
组成的.(2)不含另外两种物质的理由:
一是
Ba(OH)2遇H2SO4立刻生成沉淀
二是
Na2CO3与HNO3不能共存
.分析:根据钡离子一接触硫酸根离子就会生成沉淀,铜离子和氢氧根离子会生成氢氧化铜沉淀,加入一定体积后才出现沉淀,说明开始是在发生中和反应,所以一定存在硝酸,硝酸和碳酸钠不能共存,就不存在碳酸钠.
解答:解:氢氧化钡只要遇到硫酸就会生成沉淀,而图象是一段体积后,才开始出现沉淀,说明了一定没有硫酸,开始加入的氢氧化钡发生的是中和反应,说明存在硝酸,硝酸和碳酸钠反应,就不存在碳酸钠,还得会和氢氧化钡生成沉淀,一定存在氯化铜,
故答案为:(1)HNO3;CuCl2;
(2)Ba(OH)2遇H2SO4立刻生成沉淀;
Na2CO3与HNO3、CuCl2不能共存;
故答案为:(1)HNO3;CuCl2;
(2)Ba(OH)2遇H2SO4立刻生成沉淀;
Na2CO3与HNO3、CuCl2不能共存;
点评:在解此类题时,要学会认知图象,根据图象中的数据进行分析存在的物质和不存在的物质,然后结合推出的物质再验证其他的物质.

练习册系列答案
相关题目