题目内容
【题目】KNO3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
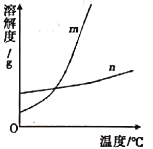
(1)依据上表数据,已绘制出KNO3和KCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是___(填"m”或“n”)。
(2)由表中数据和如图分析可知,KNO3和KCl在某一温度时具有相同的溶解度s,则s的最小取值范围是_____。
(3)某KNO3晶体中有少量KCl、Ca(OH)2杂质,要得到纯净KNO3的方法是:先加热溶解,然后_______,过滤、洗涤、干燥后得到KNO3晶体。
(4)某同学取KNO3、KCl中的一种物质,按如图所示进行实验。
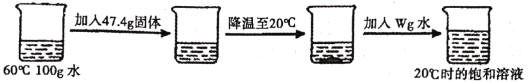
【答案】m 34.0g≤S≤37.0g 降温结晶 KNO3 50
【解析】
(1)m、n两种固体物质的溶解度,都是随温度升高而增大,而m的溶解度随温度的升高变化比n大,因此m是硝酸钾,n是氯化钾;故答案为:m;
(2)由表中数据和图1分析可知,KNO3和KCl在某一温度时具有相同的溶解度s。则s的最小取值范围是:34.0g≤S≤37.0g;故答案为:34.0g≤S≤37.0g;
(3)某KNO3晶体中有少量KCl、Ca(OH)2杂质,要得到纯净KNO3的方法是:先加热溶解、然后降温结晶、过滤、洗涤、干燥后得到KNO3晶体,因为硝酸钾的溶解度受温度的影响比较大;故答案为:降温结晶;
(4)某同学取KNO3、KCl中的一种物质,按如图所示进行实验。该同学所取的固体物质为硝酸钾,因为氯化钾的溶解度在60℃时是45.5g,烧杯中应该有剩余固体;当KNO3溶液由60℃降到20℃时,析出晶体的质量=47.4g-31.6g=15.8g,15.8g正好是31.6g的一半,因此还需要50g水;故答案为:KNO3;50。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案