题目内容
如右图所示。若在试剂瓶中放入某种物质,先滴加滴管1中液体后,小气球变鼓,再滴加滴管2中液体后,小气球又变瘪。下列与所描述现象相符的一组是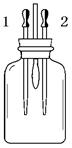
| | 试剂瓶中的物质 | 滴管中的物质 | |
| 滴管1 | 滴管2 | ||
| A | 冰 | 水 | 稀硫酸 |
| B | 稀盐酸 | 碳酸氢钠溶液 | 浓硫酸 |
| C | 生石灰 | 水 | 稀盐酸 |
| D | 二氧化碳 | 氢氧化钠溶液 | 稀盐酸 |
D
解析试题分析:若在试剂瓶中放入某种物质,先滴加滴管1中液体后,小气球变鼓,说明此时瓶内气压减小,再滴加滴管2中液体后,小气球又变瘪,此时瓶内气压又变大。若在试剂瓶中放入二氧化碳,先滴加滴管1中的氢氧化钠溶液后,二氧化碳与氢氧化钠反应生成碳酸钠和水,此时瓶内气压减小,小气球变鼓;再滴加滴管2中稀盐酸后,碳酸钠与盐酸反应产生二氧化碳气体,此时瓶内气压又变大,小气球又变瘪。选D。
考点:化学反应中的气体释放和吸收;大气压。
点评:注意理解气球变化的原因是解题关键,在试剂瓶中放入某种物质,先滴加滴管1中液体后,小气球变鼓,说明此时瓶内气压减小,再滴加滴管2中液体后,小气球又变瘪,此时瓶内气压又变大。

练习册系列答案
相关题目
如右图所示。若在试剂瓶中放入某种物质,先滴加滴管1中液体后,小气球变鼓,再滴加滴管2中液体后,小气球又变瘪。下列与所描述现象相符的一组是

|
|
试剂瓶中的物质 |
滴管中的物质 |
|
|
滴管1 |
滴管2 |
||
|
A |
冰 |
水 |
稀硫酸 |
|
B |
稀盐酸 |
碳酸氢钠溶液 |
浓硫酸 |
|
C |
生石灰 |
水 |
稀盐酸 |
|
D |
二氧化碳 |
氢氧化钠溶液 |
稀盐酸 |
 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

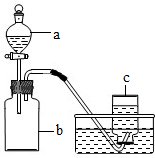 (2007?四川)某同学设计了如右图所示的装置,欲进行多种实验的探索.
(2007?四川)某同学设计了如右图所示的装置,欲进行多种实验的探索.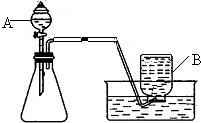 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.