题目内容
【题目】如图是我们研究常见物质组成性质的几个实验根据图示实验回答:
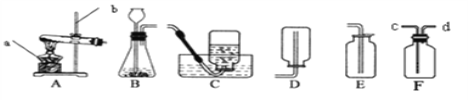
![]() 实验A集气瓶中预先装少量水的目的是______。
实验A集气瓶中预先装少量水的目的是______。
![]() 实验B中若集气瓶的容积是100mL,实验成功则量筒里的水将会减少约______mL。
实验B中若集气瓶的容积是100mL,实验成功则量筒里的水将会减少约______mL。
![]() 实验C是通过水的分解证明水的组成,a、b管内产生气体的质量比是______;科学家还用化合的方法证明水的组成,反应化学方程式为______。上述两种方法都证明了水是由氢元素和氧元素组成的化合物。
实验C是通过水的分解证明水的组成,a、b管内产生气体的质量比是______;科学家还用化合的方法证明水的组成,反应化学方程式为______。上述两种方法都证明了水是由氢元素和氧元素组成的化合物。
![]() 实验D说明:在通常情况下,二氧化碳具有的化学性质是______。
实验D说明:在通常情况下,二氧化碳具有的化学性质是______。

【答案】防止生成的高温熔化物溅落炸裂集气瓶底 20 1:8 2H2+O2![]() 2H2O 不能燃烧,不支持燃烧
2H2O 不能燃烧,不支持燃烧
【解析】
(1)铁丝在纯氧中燃烧的现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体,瓶底放少量细沙或少量的水,防止炸裂集气瓶。
(2)磷在氧气中燃烧生成五氧化二磷,空气中氧气的含量约占![]() ,故集气瓶的容积是100mL,实验成功则量筒里的水将会减少约100×
,故集气瓶的容积是100mL,实验成功则量筒里的水将会减少约100×![]() =20mL。
=20mL。
(3)水在通电的条件下生成氢气和氧气,电解水的实验中是:正氧负氢,氢二氧一;氧气能使带火星的木条复然;氢气和氧气的质量比是:(2×2):16=1:8;化合反应为两种或两种以上物质反应生成一种物质的反应,故用化合的方法证明水的组成的实验为氢气和氧气点燃生成水,化学方程式为:2H2+O2![]() 2H2O。
2H2O。
(4)如图的实验我们观察到:下层的蜡烛先熄灭,上层的蜡烛后熄灭;蜡烛熄灭说明:二氧化碳不能燃烧、不能支持燃烧;下层的蜡烛先熄灭,说明二氧化碳密度比空气的大。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】某密闭容器内有X、Y、Z、W四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | X | Y | Z | W |
反应前质量 | 4 | 1 | 10 | 2 |
反应后质量 | 待测 | 5 | 4 | 8 |
下列说法正确的是![]()
![]()
A. 反应后X的质量为8g
B. Z与W的相对分子质量比一定是1:1
C. 该反应的反应物只有Z
D. 参加反应的X与Z的质量比是2:3