题目内容
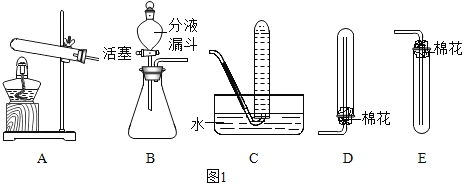
【题目】氨气易溶于水,易与浓硫酸反应,不与碱石灰(干燥剂)反应。氨气还具有还原性,在加热的条件下能将氧化铜还原为铜,同时生成氮气和水。反应的化学方程式为:2NH3+3CuO![]() N2+3Cu+3H2O,某化学小组为验证氨气的组成,设计了如下图所示实验。已知:该实验装置气密性良好,实验前装置C、D的质量分别为65.60g、132.47g,实验中所用试剂均足量。
N2+3Cu+3H2O,某化学小组为验证氨气的组成,设计了如下图所示实验。已知:该实验装置气密性良好,实验前装置C、D的质量分别为65.60g、132.47g,实验中所用试剂均足量。
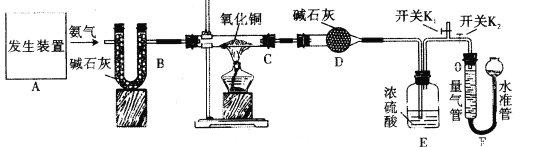
I.打开K1,关闭K2,通入氨气一段时间后,关闭K1,打开K2。(注:K1接个气球)
Ⅱ.点燃酒精灯加热,待黑色固体部分变为红色后,停止加热。
Ⅲ.继续通氨气至玻璃管冷却。
Ⅳ.记录量气管读数为VmL。
V.称量装置C、D的质量分别为65.36g、132.74g。
请回答下列问题:
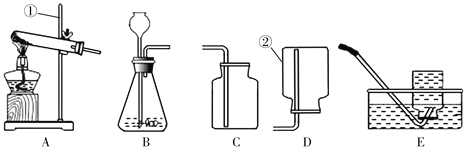
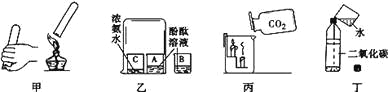
(1)若用加热氯化铵和熟石灰固体制取氨气,则发生装置与实验室制取二氧化碳气体装置_____(填“相同”或“不相同”)。
(2)步骤Ⅳ读数时,应注意视线________。
(3)反应生成水的质量为_________。
(4)实验过程中通入氨气的作用各不相同。步骤I是________________;步骤Ⅱ是还原氧化铜;步骤Ⅲ是______________________。
(5)请根据该实验数据列计算式,证明氨气中不含氧元素。相关计算式为_______________。(用题目数据表示,不需要计算)
【答案】不相同 与凹液面的最低处保持水平 0.27g 排净装置内的空气 将生成的氮气排入量气管中 65.60g-65.36g=0.27g×![]()
【解析】
(1)加热氯化铵和熟石灰固体制取氨气,选择加热固体型装置,而实验室制取二氧化碳气体的发生装置是固液常温型装置,所以发生装置不相同。
(2)步骤Ⅳ读数时,应注意视线与凹液面的最低处保持水平。
(3)装置C减少的质量是参加反应的氧化铜失去氧元素的质量,装置D增多的质量是吸收氨气的质量,该实验过程中通入氨气的质量大于参与反应的氨气质量,所以计算过程中以氧化铜减少的质量为标准进行计算,设反应生成水的质量为x,
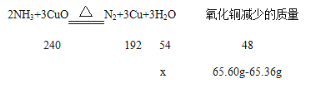
![]()
![]() =
= ![]() ,解得x=0.27g
,解得x=0.27g
(4)实验过程中通入氨气的作用各不相同。步骤I是排净装置内的空气,防止对实验的干扰;步骤Ⅱ是还原氧化铜;步骤Ⅲ是将生成的氮气排入量气管中,以减少误差。
(5)C装置中减少的质量是氧化铜中氧元素的质量,而与生成水中氧元素的质量相等,从而证明氨气中不含有氧元素:
65.60g-65.36g=0.27g×![]() ,
,