题目内容
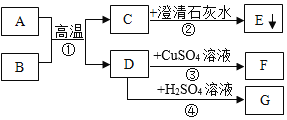
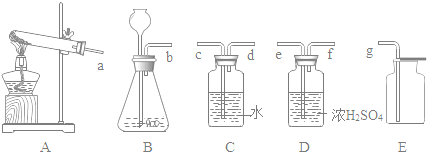
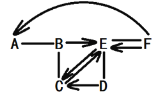
【题目】下图中A、B、C、D、E、F分别表示初中化学常见的六种物质,B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,A是目前提取量最大的金属,B由两种元素组成,C是大理石的主要成分。(图中用“—”表示两种物质之间能发生化学反应,用“→”或“![]() ”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。
”表示一种物质能转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需要在溶液中进行,物质是溶液的只考虑溶质)。
请回答下列问题。
(1)分别写出A、C、E、F物质的化学式 A______C_______E______F_______。
(2)写出B与C发生反应的化学方程式_______。
(3)写出过量A的粉末与B发生反应的实验现象_________。
【答案】 Fe CaCO3 CO2 C CaCO3+2HCl===CaCl2+H2O+CO2↑ 黑色固体减少不消失,溶液由无色变成浅绿色,固体表面有气泡冒出
【解析】A是目前提取量最大的金属,A是Fe,C是大理石的主要成分,C是 CaCO3。B由两种元素组成,既能与铁反应,又能与 CaCO3反应,则B是HCl,CaCO3![]() E,B→E,B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,C是盐,B是酸,则E是CO2,D是Ca(OH)2,F是C 。(1)A是Fe,C是CaCO3,E是CO2,F是C。(2)HCl与CaCO3发生反应的化学方程式:CaCO3+2HCl===CaCl2+H2O+CO2↑。(3)Fe +2HCl== FeCl2+H2↑,含亚铁离子的溶液是浅绿色,所以过量Fe的粉末与HCl发生反应的实验现象是,黑色固体减少不消失,溶液由无色变成浅绿色,固体表面有气泡冒出。
E,B→E,B、C、D、E分别属于酸、碱、盐、氧化物四种类别中的一种,C是盐,B是酸,则E是CO2,D是Ca(OH)2,F是C 。(1)A是Fe,C是CaCO3,E是CO2,F是C。(2)HCl与CaCO3发生反应的化学方程式:CaCO3+2HCl===CaCl2+H2O+CO2↑。(3)Fe +2HCl== FeCl2+H2↑,含亚铁离子的溶液是浅绿色,所以过量Fe的粉末与HCl发生反应的实验现象是,黑色固体减少不消失,溶液由无色变成浅绿色,固体表面有气泡冒出。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】同学们从山上采集到一种石灰石,他们取80 g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如表:
反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
反应后固体的质量m∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
请回答下列问题:
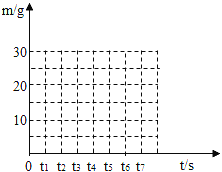
(1)当石灰石完全反应后,生成CO2的质量.
(2)求该石灰石中CaCO3的质量分数,写出计算过程.
(3)请在如图所示的坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线.