题目内容
已知每个电子的质量约为每个质子质量的1/1836,所以在科学上计算原子的
质量时只计算质子和中子的质量,电子质量忽略不计,下表是部分原子的构成指数:
通过此表,可总结出“在原子里质子数等于核外电子数”.还能总结出:
(1)
(2)
(3)
(4)
质量时只计算质子和中子的质量,电子质量忽略不计,下表是部分原子的构成指数:
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
| 铀 | 92 | 146 | 92 | 238 |
(1)
原子核内不一定都有中子
原子核内不一定都有中子
;(2)
相对原子质量=质子数+中子数
相对原子质量=质子数+中子数
;(3)
原子核内质子数不一定等于中子数
原子核内质子数不一定等于中子数
;(4)
质子数决定元素的种类
质子数决定元素的种类
.分析:根据图表所给信息去提取具有规律性的东西,有共性的东西.
解答:解:由图表可知氢原子中没有中子;相对原子质量=质子数+中子数;质子数不一定等于中子数;质子数决定元素的种类;核内质子数等于核外电子数等.
故答案为:(1)原子核内不一定都有中子;(2)相对原子质量=质子数+中子数;(3)原子核内质子数不一定等于中子数;(4)质子数决定元素的种类.
故答案为:(1)原子核内不一定都有中子;(2)相对原子质量=质子数+中子数;(3)原子核内质子数不一定等于中子数;(4)质子数决定元素的种类.
点评:根据图表总结规律时,首先要横着看有什么共同之处,和规律,再纵着看有什么共同之处和规律.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
已知每个电子的质量约为每个质子(或中子)质量的
,所以科学上在计算原子的质量时,只计算质子和中子的质量,电子的质量忽略不计.下表是部分原子的构成指数.
观察此表,可总结出“在原子里质子数等于核外电子数”,你还能总结出:
(1) ;
(2) ;
(3) .
| 1 |
| 1836 |
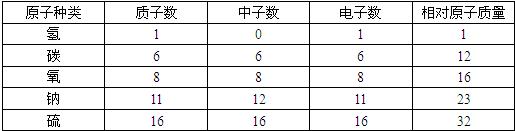
| 原子种类 | 质子数 | 中子数 | 电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
| 铀 | 92 | 146 | 92 | 238 |
(1)
(2)
(3)