题目内容
【题目】已知:![]() 。在密闭容器中,将8.8 gCO2与一定质量的Na2O2固体充分反应后,气体质量变为6.0 g。下列说法错误的是
。在密闭容器中,将8.8 gCO2与一定质量的Na2O2固体充分反应后,气体质量变为6.0 g。下列说法错误的是
A.反应物均为氧化物
B.6.0g气体中还有4.4 g的CO2
C.反应后的固体是混合物
D.生成的Na2CO3质量为10.6 g
【答案】C
【解析】
设:反应中生成氧气质量为x,碳酸钠的质量为y。
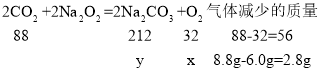
![]() x=1.6g;
x=1.6g;
![]() y=10.6g。
y=10.6g。
根据以上分析可知:
A、反应物二氧化碳和过氧化钠都是由两种元素组成,其中一种元素是氧元素的化合物,均为氧化物,故A正确;
B、6.0g气体中还有CO2的质量=6.0g-1.6g=4.4 g,故B正确;
C、根据B选项分析,反应中二氧化碳过量,过氧化钠已完全反应,反应后的固体中没有其他物质,只有碳酸钠,属于纯净物,故C错误;
D、生成的Na2CO3质量为10.6 g,故D正确。故选C。

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目