题目内容
某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数.取12.5g石灰石样品(假设杂质既不溶于水,也不与其他物质反应),向其中加入100g稀盐酸,恰好完全反应,称得烧杯内物质的质量变为108.1g.计算:
(1)该样品中碳酸钙的质量分数;
(2)所用稀盐酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数.
(1)该样品中碳酸钙的质量分数;
(2)所用稀盐酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据该反应中只有二氧化碳是气体,则利用质量守恒定律和反应前后烧杯中物质的总质量之差来计算二氧化碳的质量;将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数;
(2)根据二氧化碳的质量求出参加反应的稀盐酸中溶质的质量,进而求出所用稀盐酸中溶质的质量分数即可;
(3)利用化学反应方程式计算出氯化钙的质量,再利用溶液的质量来计算溶质的质量分数.
(2)根据二氧化碳的质量求出参加反应的稀盐酸中溶质的质量,进而求出所用稀盐酸中溶质的质量分数即可;
(3)利用化学反应方程式计算出氯化钙的质量,再利用溶液的质量来计算溶质的质量分数.
解答:解:(1)由质量守恒可知,二氧化碳的质量为12.5g+100g-108.1g=4.4g,
设碳酸钙的质量为x,参加反应的稀盐酸中溶质的质量为y,生成的氯化钙的质量为z.
则CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x y z 4.4g
=
解得x=10g
=
y=7.3g
=
z=11.1g
该样品中碳酸钙的质量分数为
×100%=80%
(2)所用稀盐酸中溶质的质量分数=
×100%=7.3%
(3)因杂质既不溶于水,也不与其他物质反应,则溶液的质量为108.1g-(12.5g-10g)=106g,溶质的质量为11.1g,
则溶质的质量分数为
×100%=10.5%
答:(1)该样品中碳酸钙的质量分数为80%;
(2)所用稀盐酸中溶质的质量分数为7.3%;
(3)反应后所得溶液中溶质的质量分数为10.5%.
设碳酸钙的质量为x,参加反应的稀盐酸中溶质的质量为y,生成的氯化钙的质量为z.
则CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x y z 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
解得x=10g
| 73 |
| y |
| 44 |
| 4.4g |
y=7.3g
| 111 |
| z |
| 44 |
| 4.4g |
z=11.1g
该样品中碳酸钙的质量分数为
| 10g |
| 12.5g |
(2)所用稀盐酸中溶质的质量分数=
| 7.3g |
| 100g |
(3)因杂质既不溶于水,也不与其他物质反应,则溶液的质量为108.1g-(12.5g-10g)=106g,溶质的质量为11.1g,
则溶质的质量分数为
| 11.1g |
| 106g |
答:(1)该样品中碳酸钙的质量分数为80%;
(2)所用稀盐酸中溶质的质量分数为7.3%;
(3)反应后所得溶液中溶质的质量分数为10.5%.
点评:本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
相关题目
相同质量的SO2与SO3中,氧元素的质量比是( )
| A、2:3 | B、1:1 |
| C、5:6 | D、7:12 |
 盐酸.为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A、B、C进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如图所示的探究活动:
盐酸.为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A、B、C进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如图所示的探究活动: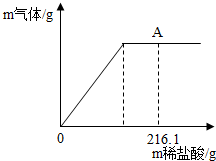 向盛有22.3g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入质量分数为10%的稀盐酸,放出气体的质量与滴入稀盐酸的质量关系如图所示.反应结束后,A点氯化钠溶质的质量分别为10%.求算:
向盛有22.3g碳酸钠和氯化钠固体混合物的烧杯中逐滴加入质量分数为10%的稀盐酸,放出气体的质量与滴入稀盐酸的质量关系如图所示.反应结束后,A点氯化钠溶质的质量分别为10%.求算: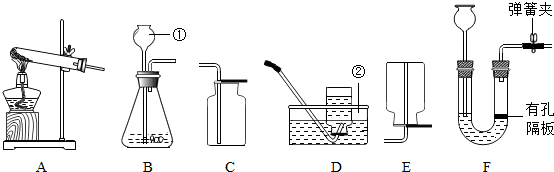
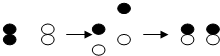 如图表示氢气(H2)和氯气(Cl2)反应生成氯化氢(HCl)的示意图,根据以下信息回答:
如图表示氢气(H2)和氯气(Cl2)反应生成氯化氢(HCl)的示意图,根据以下信息回答: