题目内容
【题目】取一定质量的石灰石(所含杂质不溶于水,不与酸反应,高温也不分解),高温煅烧一段时间后,将所得固体与200 g溶质质量分数为14.6%的稀盐酸充分反应,过滤得到10 g滤渣和一定质量的中性溶液,则原石灰石中碳酸钙的质量分数是
A. 80.0% B. 83.8% C. 74.4% D. 92.6%
【答案】A
【解析】200g质量分数为14.6%的稀盐酸中所含氯元素质量=200g×14.6%×![]() ×100%=28.4g
×100%=28.4g
氯化钙中钙元素与氯元素质量比=40:(35.5×2)=40:71,则氯化钙中氯元素质量为28.4g时钙元素质量=![]() ×40=16g
×40=16g
石灰石中碳酸钙的质量=16g÷(![]() ×100%)=40g,依据题意可知过滤所得的滤渣即为原石灰石中的杂质;
×100%)=40g,依据题意可知过滤所得的滤渣即为原石灰石中的杂质;
则原石灰石样品中碳酸钙的质量分数![]() ×100%=80%。
×100%=80%。

 新思维寒假作业系列答案
新思维寒假作业系列答案【题目】草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
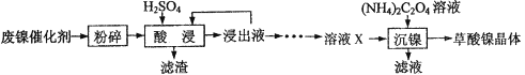
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
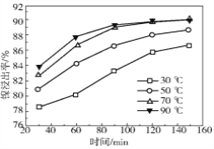
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。