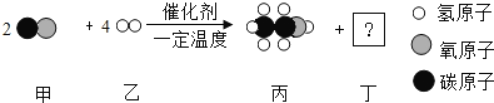
题目内容
【题目】请回答下列实验问题:

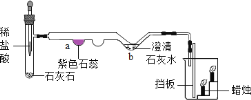
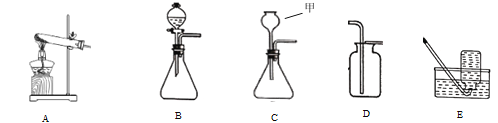
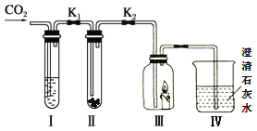
用如图所示装置探究燃烧的条件:
A 现象①③说明________
B 现象①②说明________
C 古语道:“人要实,火要虚”。从燃烧的条件看,“火要虚”的实质________
【答案】可燃物与氧气接触 温度必达到可燃物的着火点 增大可燃物与O2的接触面积,燃烧更剧烈
【解析】
实验中,①处的白磷既与氧气接触,温度又达到了白磷的着火点,所以发生了燃烧;②处的红磷虽然与氧气接触,但是温度没有达到其着火点,所以没有发生燃烧;③处的白磷温度虽然温度到了其着火点,但是没有与氧气接触,所以也没有发生燃烧。
A、现象①③说明燃烧的条件之一是可燃物与氧气接触;
B、现象①②说明燃烧的条件之一是温度必须达到可燃物的着火点;
C、“火要虚”的实质就是增大可燃物与空气的接触面积,促进燃料的燃烧。

【题目】钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.某化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]A.Ti>Mg>Ag; B.Mg>Ag>Ti; C._____.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.请填空:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_____.
(2)根据下表中的实验现象填空:
Ti | Mg | Ag | |
实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
[结论]假设_____正确(填“A”或“B”或“C”)
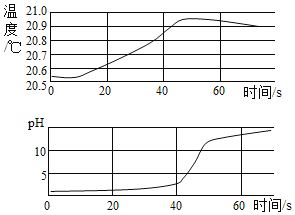
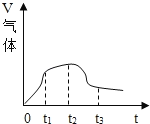
(3)在做镁条与稀盐酸反应过程中观察到产生气体体积与反应时间有如图所示关系:
则t1~t2时间内反应速率逐渐加快的主要原因是_____. t2~t3时间内反应速率逐渐减慢的原因是_____.
(4)在[实验设计]中,如果所用盐酸的溶质质量分数不同,是否一定能够得出正确结论?_____(填“是”或“否”),理由是_____.
(5)你是否还知道其他方法来比较这三种金属的活动性(可供选择的药品:Ti、Mg、Ag、TiCl2溶液、MgCl2溶液、AgNO3溶液).
①_____;②_____.