题目内容
【题目】鸡蛋壳的主要成分是碳酸钙,某同学为了测定鸡蛋壳中碳酸钙的质量分数,设计了如图实验并进行计算,将鸡蛋壳洗净、干燥并捣碎后放入锥形瓶里,加入足量的稀盐酸充分反应(假定其他杂质不与盐酸反应),测得相关数据如图所示:
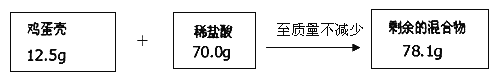
【数据处理】
(1)二氧化碳的质量_____.
(2)计算鸡蛋壳中碳酸钙的质量分数为_______,并写出计算过程.
【答案】 4.4g 80%
【解析】解:根据质量守恒定律,二氧化碳的质量为:12.5g+70.0g-78.1g=4.4g;
设该鸡蛋壳样品中碳酸钙的质量分数为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
12.5gx 4.4g
![]()
x=80%
答: (1)二氧化碳的质量 4.4g;
(2)鸡蛋壳中碳酸钙的质量分数为 80%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目