题目内容
【题目】在实验室里,小明与同学欲用如图所示装置(气密性良好)和药品制取初中化学常见气体并验证其有关性质
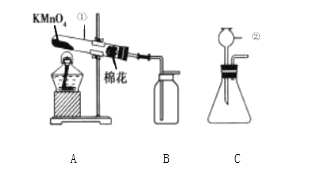
(1)写出图中标有序号的仪器②的名称:________________
(2)点燃 A 中的酒精灯制取并收集氧气, 用装置 A 制取氧气化学方程式为______________,检验 B 中氧气已收集满的方法是_____________________
(3)将点燃的蜡烛放入集满氧气的集气瓶中,可观察到 , 且瓶壁上有水雾出现,证明蜡烛燃烧有水生成。接着,将蜡烛从集气瓶中取出,___________________(填实验步骤和现象),证明蜡烛燃烧还生成了二氧化碳。
(4)小明同学发现装置C有一处明显错误:_______________,将装置 C 改正后放入适量的药品,即又开始制取氧气,化学方程式为________________
【答案】 长颈漏斗 2KMnO4![]() K2MnO4+MnO2+O2↑ 用带火星的木条伸到集气瓶口,若木条复燃则说明氧气已集满 向集气瓶倒入适量澄清石灰水,振荡,石灰水变浑浊 长颈漏斗的末端未接近锥形瓶的底部 2H2O2
K2MnO4+MnO2+O2↑ 用带火星的木条伸到集气瓶口,若木条复燃则说明氧气已集满 向集气瓶倒入适量澄清石灰水,振荡,石灰水变浑浊 长颈漏斗的末端未接近锥形瓶的底部 2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
【解析】(1)标有序号的仪器名称为②长颈漏斗;(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是:2KMnO4![]() K2MnO4+MnO2+O2↑,检验 B 中氧气已收集满的方法是用带火星的木条伸到集气瓶口,若木条复燃则说明氧气已集满;(3)蜡烛在氧气中燃烧的更旺,发出白光,放出热量,将澄清的石灰水倒入集气瓶后,振荡,若变浑浊,则证明生成了二氧化碳;(4)该装置中,长颈漏斗的末端没有接近锥形瓶的底部,会导致生成的气体从长颈漏斗逸出,该装置适用于固液常温下来制取气体,如用锌粒与稀硫酸来制取氢气、过氧化氢在二氧化锰的催化作用下制取氧气、大理石或石灰石与稀盐酸反应来制取二氧化碳;如加热的药品为过氧化氢和二氧化锰,反应的方程式为:2H2O2
K2MnO4+MnO2+O2↑,检验 B 中氧气已收集满的方法是用带火星的木条伸到集气瓶口,若木条复燃则说明氧气已集满;(3)蜡烛在氧气中燃烧的更旺,发出白光,放出热量,将澄清的石灰水倒入集气瓶后,振荡,若变浑浊,则证明生成了二氧化碳;(4)该装置中,长颈漏斗的末端没有接近锥形瓶的底部,会导致生成的气体从长颈漏斗逸出,该装置适用于固液常温下来制取气体,如用锌粒与稀硫酸来制取氢气、过氧化氢在二氧化锰的催化作用下制取氧气、大理石或石灰石与稀盐酸反应来制取二氧化碳;如加热的药品为过氧化氢和二氧化锰,反应的方程式为:2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。

【题目】下面是兴趣小组同学对暴露在空气的氢氧化钠固体的探究.请回答下列问题:
[提出问题1]: 该氢氧化钠固体有没有变质呢?
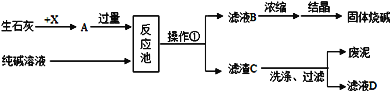
[进行实验1]:甲同学取少量固体于试管中用足量的水溶解,后加入过量的 BaCl2 溶液,观察到_________________,证明氢氧化钠固体已经含有 Na2CO3.
[提出问题2]:
如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
[进行实验2]:乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验.
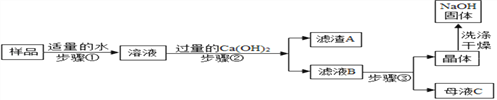
[实验分析]:
⑴步骤②反应的化学方程式是____________,步骤②的操作有搅拌和过滤,搅拌的作用是_______.
⑵证明步骤②中已达到 Ca(OH)2溶液过量的目的,下列方案中可行的是_________.
a.取少量滤液 B,向其中通二氧化碳气体,溶液变浑浊
b.取少量溶液 B,向其中再加少量石灰水,无白色浑浊
c.取少量溶液 B,向其中再加少量浓碳酸钠溶液,有白色浑浊
⑶为获得纯净的氢氧化钠步骤③所包含的具体操作是蒸发浓缩、_________、过滤. A.蒸发结晶B.降温结晶
⑷丙同学认为乙同学流程中的 Ca(OH)2 溶液可以用稍过量的 Ba(OH)2 溶液代替,代替后的主要优点是_______________.
A.氢氧化钙微溶于水,氢氧化钡易溶于水,用氢氧化钡溶液可以减少溶液中水的量,以提高蒸发浓缩的效率,并节约能源.
B.只有氢氧化钡才能除去杂质
[实验拓展]:如何测定久置的烧碱样品中氢氧化钠的质量分数呢?
从一瓶久置的烧碱中称取了 20g,干燥后剩余固体固体质量为 19g,完全溶于蒸馏水 中配成 100g 样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反 应后得到如表所示的数据.
项目和次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 |
样品溶液质量(g) | 10 | 20 | 30 | 40 |
氯化钡溶液质量(g) | 10 | 15 | 15 | 30 |
产生沉淀的质量(g) | 1.97 | 3.94 | 3.94 | X |
⑸表中第_________次恰好完全反应.
⑹请计算样品中氢氧化钠的质量分数为_____________?(请写具体解题过程)