题目内容
某化学兴趣小组对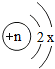 粒子进行探究.下列结论中,错误的是( )
粒子进行探究.下列结论中,错误的是( )
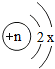 粒子进行探究.下列结论中,错误的是( )
粒子进行探究.下列结论中,错误的是( )| A、当x=6时且该粒子为原子时,核电荷数n应为8 |
| B、当x=8时且该粒子为阴离子时,核电荷数n应为12 |
| C、当n=11时且该粒子为阳离子时,x应为8 |
| D、当x=8时,该粒子的化学性质较稳定 |
考点:原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:A、利用原子中质子数等于核外电子数,进行判断;
B、利用原子得电子形成带电的阴离子,因此,阴离子中核外电子数大于质子数;
C、当原子的最外层电子数小于4时,易失去最外层电子而变成阳离子;
D、根据最外层电子数=8,(第一层=2)时是排满的结构,是稳定结构解答.
B、利用原子得电子形成带电的阴离子,因此,阴离子中核外电子数大于质子数;
C、当原子的最外层电子数小于4时,易失去最外层电子而变成阳离子;
D、根据最外层电子数=8,(第一层=2)时是排满的结构,是稳定结构解答.
解答:解:A、当该粒子表示为原子时,质子数等于核外电子数,因此,当x=6时核电荷数n为8;故A正确;
B、当该粒子表示为阴离子时,核外电子数大于质子数,因此,当x=8时核电荷数n应小于10;故B错误;
C、当该粒子表示为阳离子时,当n=11时,该粒子的原子核外电子分三层且最外层电子数为1小于4而失电子,因此,x为8;故C正确;
D、当x=8时,是稳定结构,故该粒子的化学性质较稳定;故D正确;
故选B.
B、当该粒子表示为阴离子时,核外电子数大于质子数,因此,当x=8时核电荷数n应小于10;故B错误;
C、当该粒子表示为阳离子时,当n=11时,该粒子的原子核外电子分三层且最外层电子数为1小于4而失电子,因此,x为8;故C正确;
D、当x=8时,是稳定结构,故该粒子的化学性质较稳定;故D正确;
故选B.
点评:在原子的结构示意图中,质子数等于核外电子数,当最外层电子数小于4时易失电子而形成阳离子,当最外层电子数大于4时易得电子而形成阴离子.

练习册系列答案
相关题目
“绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%.在用C3H4(丙炔)合成C5H8O2(2-甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
| A、CH4和H2O |
| B、CH3OH和H2 |
| C、CO和CH3OH |
| D、CH4和HCHO |
某研究小组测定Cu-Fe合金和Fe-Al合金中铁的质量分数.向5.6g其中一种合金粉末中加入100g某溶质质量分数的稀硫酸,恰好完全反应,并产生ag氢气,则下列说法正确的是( )
| A、当粉末为Fe-Al合金时,a可能为0.2g |
| B、当粉末为Cu-Fe合金时,反应完全后,生成物的溶液里一定含有Fe2+和Cu2+ |
| C、当粉末为Cu-Fe合金时,若a为0.1g,则该种合金中含铁的质量分数为50% |
| D、当粉末为Fe-Al合金时,所需稀硫酸溶质质量分数一定大于或等于9.8% |
下列实验操作正确的是( )
A、 |
B、 |
C、 |
D、 |
二氧化碳是一种无色无味的气体,密度比空气大,且能溶于水,收集二氧化碳时可选用的收集方法是( )
| A、向上排空气法 |
| B、向下排空气法 |
| C、排水法 |
| D、排水法或向上排空气法 |
决定元素种类的是( )
| A、中子 | B、电子 |
| C、核电荷数或者质子数 | D、最外层电子数 |
下列有关酒精灯使用或存放的图示错误的是( )
A、 点燃酒精灯 |
B、 添加酒精 |
C、 存放酒精灯 |
D、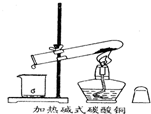 加热碱式碳酸铜 |
下列仪器能直接用来加热的玻璃仪器是( )
| A、集气瓶 | B、蒸发皿 |
| C、烧杯 | D、试管 |
以下说法正确的是( )
| A、中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 |
| B、中和反应后的溶液一定显中性 |
| C、碱中都含有氢元素,所以含有氢元素的化合物一定是碱 |
| D、能使酚酞试液变红的溶液是碱性溶液 |