题目内容
某研究小组测定Cu-Fe合金和Fe-Al合金中铁的质量分数.向5.6g其中一种合金粉末中加入100g某溶质质量分数的稀硫酸,恰好完全反应,并产生ag氢气,则下列说法正确的是( )
| A、当粉末为Fe-Al合金时,a可能为0.2g |
| B、当粉末为Cu-Fe合金时,反应完全后,生成物的溶液里一定含有Fe2+和Cu2+ |
| C、当粉末为Cu-Fe合金时,若a为0.1g,则该种合金中含铁的质量分数为50% |
| D、当粉末为Fe-Al合金时,所需稀硫酸溶质质量分数一定大于或等于9.8% |
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:因为铝的相对原子质量比铁小,所以相同质量的铝与酸完全反应时,产生的氢气质量多,而铜与酸不反应,所以可以将铜的相对原子质量看成无限大.
解答:解:
A、假设合金中铁的质量为5.6 g,则根据化学反应的方程式:Fe+H2SO4=FeSO4+H2↑可计算出此时产生氢气的质量为0.2 g,同理可计算出5.6 gAl与足量硫酸反应产生氢气的质量大于0.2 g,因此当粉末为Fe-Al合金时,a>0.2 g;
B、铜不与硫酸反应产生氢气,因此当粉末为Cu-Fe合金时,a<0.2 g,生成物的溶液里没有Cu2+;
C、当粉末为Cu-Fe合金时若a为0.1g时,利用化学方程式可计算出需铁的质量为2.8g,故该种合金中含铁的质量分数为50%;
D、当粉末为Fe-Al合金时,因相同质量的铝消耗硫酸的质量比铁消耗硫酸的质量大,而5.6 g铁时,消耗硫酸的质量为9.8 g,所以合金为为Fe-Al合金时,所需稀硫酸溶质质量分数一定大于9.8%.
答案;CD
A、假设合金中铁的质量为5.6 g,则根据化学反应的方程式:Fe+H2SO4=FeSO4+H2↑可计算出此时产生氢气的质量为0.2 g,同理可计算出5.6 gAl与足量硫酸反应产生氢气的质量大于0.2 g,因此当粉末为Fe-Al合金时,a>0.2 g;
B、铜不与硫酸反应产生氢气,因此当粉末为Cu-Fe合金时,a<0.2 g,生成物的溶液里没有Cu2+;
C、当粉末为Cu-Fe合金时若a为0.1g时,利用化学方程式可计算出需铁的质量为2.8g,故该种合金中含铁的质量分数为50%;
D、当粉末为Fe-Al合金时,因相同质量的铝消耗硫酸的质量比铁消耗硫酸的质量大,而5.6 g铁时,消耗硫酸的质量为9.8 g,所以合金为为Fe-Al合金时,所需稀硫酸溶质质量分数一定大于9.8%.
答案;CD
点评:相同质量的金属与酸反应产生氢气的质量的多少与金属的相对原子质量有关.若相对原子质量越大,产生的氢气质量越小.

练习册系列答案
相关题目
下列叙述正确的是( )
①分子是保持物质性质的一种微粒
②原子是不能再分的一种微粒
③有单质生成的反应一定是置换反应
④生成两种化合物的反应一定是复分解反应
⑤含有氧元素的化合物一定是氧化物
⑥由不同种元素组成的纯净物一定是化合物
⑦高炉炼铁原理为2Fe2O3+3C
4Fe+3CO2↑
①分子是保持物质性质的一种微粒
②原子是不能再分的一种微粒
③有单质生成的反应一定是置换反应
④生成两种化合物的反应一定是复分解反应
⑤含有氧元素的化合物一定是氧化物
⑥由不同种元素组成的纯净物一定是化合物
⑦高炉炼铁原理为2Fe2O3+3C
| ||
| A、①③④ | B、⑥⑦ |
| C、⑥ | D、②④⑤⑥ |
下列气体遇到明火可能爆炸的是( )
| A、氧气和氮气 |
| B、氢气和氮气 |
| C、纯净的氢气 |
| D、氧气和氢气 |
下列变化属于分解反应的是( )
A、氢气+氧化铜
| ||
B、氧气+氢气
| ||
C、碳酸钙
| ||
D、酒精+氧气
|
用量筒量取10mL水时仰视读数,则所量水的实际体积是( )
| A、10mL |
| B、大于10mL |
| C、小于10mL |
| D、无法确定 |
下列对实验现象的描述正确的是( )
| A、红磷在空气中燃烧产生大量白雾 |
| B、蜡烛在空气中燃烧生成二氧化碳和水 |
| C、铁丝在氧气中燃烧时火星四射、生成黑色固体 |
| D、硫在空气中燃烧生成有刺激性气味的二氧化硫 |
某化学兴趣小组对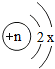 粒子进行探究.下列结论中,错误的是( )
粒子进行探究.下列结论中,错误的是( )
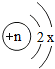 粒子进行探究.下列结论中,错误的是( )
粒子进行探究.下列结论中,错误的是( )| A、当x=6时且该粒子为原子时,核电荷数n应为8 |
| B、当x=8时且该粒子为阴离子时,核电荷数n应为12 |
| C、当n=11时且该粒子为阳离子时,x应为8 |
| D、当x=8时,该粒子的化学性质较稳定 |
下列对空气的描述正确的是( )
| A、按质量分数计算,空气中氧气约占78%,氮气约占21% |
| B、空气的成分是固定不变的 |
| C、空气是纯净物 |
| D、空气的成分是比较固定的,主要由氧气和氮气组成 |