题目内容
(1)如图是我们在实验室制取物质和进行物质性质实验的常用装置.请按要求回答下面的问题:

①检查装置B气密性的方法是______
②若在实验室中制得一瓶氧气,你选择的化学反应是______(化学方程式表示),选用的装置是______(填序号);
③使用锌和稀盐酸制取氢气,可选用的发生装置有______(填序号),产生的气体经装置______(填序号)分别除去少量______的和______,即可得到纯净干燥的氢气.
(2)二氧化锰对许多化学反应都有催化作用.小明同学在完成某实验后,发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,为进一步探究这时的二氧化锰是否仍有催化作用,小明将其分离回收,并想通过实验进行探究.请你帮他设计实验并回答下面问题:
①简述你的实验方法______;
②在该实验中观察到的现象是______;
③根据实验现象,你得到的结论是______;
④通过探究,你对催化剂的认识是______.
解:(1)①检查装置B气密性的方法是:从长颈漏斗中注水使漏斗下端浸没在水面下后,后用止水夹将导气管夹紧密封,手捂锥形瓶加热至液面上升,一段时间不回落表明气密性良好;
②若在实验室中制得一瓶氧气,你选择的化学反应是:2H2O2 2H2O+O2↑;根据反应原理、气密性选择装置:B、G
2H2O+O2↑;根据反应原理、气密性选择装置:B、G
③使用锌和稀盐酸制取氢气,可选用的发生装置有:B、C;产生的气体经装置E、D分别除去少量氯化氢和水蒸气,即可得到纯净干燥的氢气.
(2)探究发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,在完成某实验后的二氧化锰是否仍有催化作用,小明将其分离回收:①简述你的实验方法:在一支洁净的试管中注入2mL双氧水,观察现象;加入少量回收的二氧化锰后,继续观察现象;
②在该实验中观察到的现象是:加入二氧化锰后,产生气泡的速度明显加快;
③根据实验现象,你得到的结论是:回收的二氧化锰仍具有催化作用;
④通过探究,你对催化剂的认识是:催化剂在化学反应前后,其化学性质不变,可以重复使用.
故答为:(1)①从长颈漏斗中注水使漏斗下端浸没在水面下后,后用止水夹将导气管夹紧密封,手捂锥形瓶加热至液面上升,一段时间不回落表明气密性良好;②2H2O2 2H2O+O2↑;B、G;③B、C;E、D;氯化氢;水蒸气
2H2O+O2↑;B、G;③B、C;E、D;氯化氢;水蒸气
说明:①、②小题中,其他合理答案也可按标准赋分.
(2)①在一支洁净的试管中注入2mL双氧水,观察现象;加入少量回收的二氧化锰后,继续观察现象;
②加入二氧化锰后,产生气泡的速度明显加快;
③回收的二氧化锰仍具有催化作用;
④催化剂在化学反应前后,其化学性质不变,可以重复使用.
说明:本题有几个不同方案,任一合理方案均可按标准赋分.
分析:(1)①掌握检查装置B气密性的方法;②制取氧气,选择简单、易操作的进行;根据气密性和水溶性,选择收集装置;③用锌和稀盐酸制取氢气:类比制取二氧化碳的装置制取;因为氯化氢易挥发,用氢氧化钠溶液吸收氯化氢气体;水蒸气用浓硫酸吸收;
(2)探究发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,在完成某实验后的二氧化锰是否仍有催化作用,小明将其分离回收:①设计合理的实验;②描述现象;③得出结论;④对催化剂“一变二不变”,再次认识.
点评:根据气体反应原理和气密性和水溶性制取选取装置;学会检查装置的气密性的方法;根据题意正确书写化学方程式.
②若在实验室中制得一瓶氧气,你选择的化学反应是:2H2O2
 2H2O+O2↑;根据反应原理、气密性选择装置:B、G
2H2O+O2↑;根据反应原理、气密性选择装置:B、G③使用锌和稀盐酸制取氢气,可选用的发生装置有:B、C;产生的气体经装置E、D分别除去少量氯化氢和水蒸气,即可得到纯净干燥的氢气.
(2)探究发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,在完成某实验后的二氧化锰是否仍有催化作用,小明将其分离回收:①简述你的实验方法:在一支洁净的试管中注入2mL双氧水,观察现象;加入少量回收的二氧化锰后,继续观察现象;
②在该实验中观察到的现象是:加入二氧化锰后,产生气泡的速度明显加快;
③根据实验现象,你得到的结论是:回收的二氧化锰仍具有催化作用;
④通过探究,你对催化剂的认识是:催化剂在化学反应前后,其化学性质不变,可以重复使用.
故答为:(1)①从长颈漏斗中注水使漏斗下端浸没在水面下后,后用止水夹将导气管夹紧密封,手捂锥形瓶加热至液面上升,一段时间不回落表明气密性良好;②2H2O2
 2H2O+O2↑;B、G;③B、C;E、D;氯化氢;水蒸气
2H2O+O2↑;B、G;③B、C;E、D;氯化氢;水蒸气说明:①、②小题中,其他合理答案也可按标准赋分.
(2)①在一支洁净的试管中注入2mL双氧水,观察现象;加入少量回收的二氧化锰后,继续观察现象;
②加入二氧化锰后,产生气泡的速度明显加快;
③回收的二氧化锰仍具有催化作用;
④催化剂在化学反应前后,其化学性质不变,可以重复使用.
说明:本题有几个不同方案,任一合理方案均可按标准赋分.
分析:(1)①掌握检查装置B气密性的方法;②制取氧气,选择简单、易操作的进行;根据气密性和水溶性,选择收集装置;③用锌和稀盐酸制取氢气:类比制取二氧化碳的装置制取;因为氯化氢易挥发,用氢氧化钠溶液吸收氯化氢气体;水蒸气用浓硫酸吸收;
(2)探究发现用作催化剂二氧化锰的颜色、状态均未发生明显变化,在完成某实验后的二氧化锰是否仍有催化作用,小明将其分离回收:①设计合理的实验;②描述现象;③得出结论;④对催化剂“一变二不变”,再次认识.
点评:根据气体反应原理和气密性和水溶性制取选取装置;学会检查装置的气密性的方法;根据题意正确书写化学方程式.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
(1)探究物质的性质
如右图所示,小文同学将酚酞溶液分别倒入A、B两个小烧杯中,另取一个小烧杯C,加入约5 mL浓氨水。用一个大烧杯罩住A、C两个小烧杯。
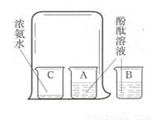
①我能观察到的实验现象 ;
②B烧杯在实验中是不可缺少的,它体现出的一种科学实[来源:Zxxk.Com]
验方法是 。
(2)探究物质的用途
水是同学们非常熟悉的物质之一。它与我们人类的关系非常密切,在生产、生活和科学实验中有广泛的用途。下面三个实验中都用到水,我能说明水的作用。

A、硫在氧气中燃烧 B、铁丝在氧气中燃烧 C、电解水
①三个实验中水的作用各不相同,我能一一说出。
A瓶中的水: 。B瓶中的水: 。C水槽中的水: 。
②王磊做电解水的实验时,用铜丝做导线和电极,得到氢气和氧气的体积比为2.2:1,和理论值相比有误差,请你从所得气体的两个不同性质的层面上分析原因: 、 。
(3)探究物质的组成
艾化学同学以木条为基本原料,进行了如下一系列探究实验:
|
实验操作 |
实验现象 |
实验结论 |
方法提炼 |
|
点燃干燥的木条,在火焰上方罩干冷的烧杯 |
一会儿烧杯内壁有水雾产生。 |
木条中一定含有 元素 |
根据一切化学反应中元素的 不变,同时根据表格中的实验 可以推测出实验结论。 |
|
继续把火焰靠近烧杯底部[来源:ZXXK] |
一会儿烧杯底部出现一层黑色物质 |
木条中一定含有 元素[来源:ZXXK] |
(2010?广安)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂.
【提出猜想】淡黄色粉末可能是:a.硫; b.过氧化钠; c.硫和过氧化钠的混合物.
【实验探究一】过氧化钠与水反应的生成物是什么?
(1)取适量的该粉末于试管中,加入足量蒸馏水产生气泡,证明猜想______不成立;
(2)用带火星的木条伸入反应的试管中,木条复燃,说明产生______;
(3)充分反应后,试管中只得到无色溶液;向溶液中滴加______,观察到______,证明生成物中有NaOH;同时证明猜想______成立.
(4)写出过氧化钠与水反应的化学方程式:______.
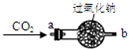
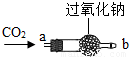
【实践探究二】过氧化钠为什么能作供氧剂?大家讨论认为可能是CO2在常温下能与过氧
化钠反应有关,于是设计如图所示的装置继续实验探究.
【实验结论】CO2在常温下能与过氧化钠反应,该反应的化学方程式为:______
【交流比较】与我们学过的用KClO3或KMnO4制取氧气的方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是(从两个不同角度回答):______、______.
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂.
【提出猜想】淡黄色粉末可能是:a.硫; b.过氧化钠; c.硫和过氧化钠的混合物.
【实验探究一】过氧化钠与水反应的生成物是什么?
(1)取适量的该粉末于试管中,加入足量蒸馏水产生气泡,证明猜想______不成立;
(2)用带火星的木条伸入反应的试管中,木条复燃,说明产生______;
(3)充分反应后,试管中只得到无色溶液;向溶液中滴加______,观察到______,证明生成物中有NaOH;同时证明猜想______成立.
(4)写出过氧化钠与水反应的化学方程式:______.
【实践探究二】过氧化钠为什么能作供氧剂?大家讨论认为可能是CO2在常温下能与过氧
化钠反应有关,于是设计如图所示的装置继续实验探究.
| 实 验 操 作 | 实 验 现 象 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的气体通入澄清石灰水中 | 有气泡产生, 石灰水变浑浊 |
【交流比较】与我们学过的用KClO3或KMnO4制取氧气的方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是(从两个不同角度回答):______、______.