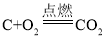题目内容
【题目】氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
制氢:铁酸锌( ZnFe2O4)可用于循环分解水制氢,其反应可表示为:
![]() ;
;![]()
(1) ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢的过程中,不断被消耗的物质是_____(填化学式)。
(3)氢气作为新能源的优点有_____(任写一点),该循环法制氢的不足之处是_____。
(4)下列说法正确的是_____(填序号)。
A 能源结构向多元、清洁、低碳转型
B 科技进步会促进能源的利用
C 石油和太阳能属于可再生能源
D 生活中的废热可转化为电能
【答案】+3 H2O 燃烧产物为水,无污染 所需温度高,消耗能源多等 ABD
【解析】
在化合物中各元素的化合价代数和为零。
(1) ZnFe2O4中锌元素的化合价为+2价,氧元素的化合价为-2价,设 Fe的化合价为x,化合物中各元素的化合价代数和为零,![]() ,x=+3,故Fe的化合价为+3价。
,x=+3,故Fe的化合价为+3价。
(2)该循环制氢的过程中,铁酸锌( ZnFe2O4)可用于循环分解水制氢,不断被消耗的物质是水,化学式为H2O。
(3)氢气在氧气中点燃生成水,氢气作为新能源的优点有燃烧产物为水,无污染,该循环法制氢的不足之处是所需温度高,消耗能源多等。
(4)A、氢能源无污染,能源结构向多元、清洁、低碳转型,故A正确;
B、科技进步会促进能源的利用,故B正确;
C、太阳能属于可再生能源,石油属于不可再生能源,故C不正确;
D、生活中的废热可转化为电能,故D正确。故选ABD。

【题目】在一定条件下,向一密闭的容器内加入A、B、C、D四种物质各20g,充分反应后,测定其质量,得到数据如下:
物质 | A | B | C | D |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 未知 | 14 |
(1)反应后C的质量是_____g。
(2)A物质可能是_____(填“反应物”或“生成物”“催化剂”)。
(3)容器中B物质肯定是_____填“单质”或“化合物”)。
(4)容器中发生反应的基本反应类型是_____。