题目内容
某镁铝合金的样品7.2 g,研成粉末后与200 g稀盐酸恰好完全反应,则稀盐酸的溶质质量分数可能是
| A.18.25% | B.14.6% |
| C.12% | D.3.6 % |
C
①设7.2g全是镁,此时消耗盐酸质量最少,则消耗盐酸的质量为x,
Mg+2HCl=MgCl2+H2↑
24 73
7.2g x

解之得:x=21.9g,
则该盐酸的质量分数为: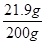 ×100%≈11.0%;
×100%≈11.0%;
②如果全是Al,此时消耗盐酸质量最大,则消耗盐酸质量为y,
2Al+6HCl=2AlCl3+3H2↑
54 219
7.2g y
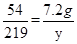
解之得:y=29.2g,
则该盐酸的质量分数为: ×100%=14.6%.
×100%=14.6%.
所以盐酸质量分数在11.0%和14.6%之间.
故选C.
Mg+2HCl=MgCl2+H2↑
24 73
7.2g x

解之得:x=21.9g,
则该盐酸的质量分数为:
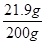 ×100%≈11.0%;
×100%≈11.0%;②如果全是Al,此时消耗盐酸质量最大,则消耗盐酸质量为y,
2Al+6HCl=2AlCl3+3H2↑
54 219
7.2g y
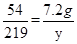
解之得:y=29.2g,
则该盐酸的质量分数为:
 ×100%=14.6%.
×100%=14.6%.所以盐酸质量分数在11.0%和14.6%之间.
故选C.

练习册系列答案
相关题目
 2NaOH + Cl2↑+ H2↑
2NaOH + Cl2↑+ H2↑