题目内容
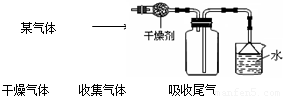
如图是收集某气体的装置.由实验装置推测该气体的有关性质正确的是| A | B | C | D | |
| 密度比空气 | 大 | 大 | 小 | 小 |
| 水中的溶解性 | 难溶 | 易溶 | 易溶 | 难溶 |
A.A
B.B
C.C
D.D
【答案】分析:根据图中收集气体的方法可知,空气是从底部的长管排出来的,再进一步分析该气体的密度大小;根据气体的尾气吸收是用水,来分析该气体的溶解性.
解答:解:图中是利用排空气法收集气体,由图示可知空气是从底部的长管排出来的,说明该气体是聚集在上方,把空气排到底部从长管排出,所以该气体的密度比空气密度小;气体的尾气吸收是用水,说明该气体易溶于水,否则水就不能吸收该气体了,所以该气体密度比空气小,易溶于水.
故选C.
点评:易溶于水的气体可以用水来吸收,密度比空气大用向上排空气法收集,密度比空气小用向下排空气法收集,由图示可知空气从下端被排出,相当于向下排空气法收集.
解答:解:图中是利用排空气法收集气体,由图示可知空气是从底部的长管排出来的,说明该气体是聚集在上方,把空气排到底部从长管排出,所以该气体的密度比空气密度小;气体的尾气吸收是用水,说明该气体易溶于水,否则水就不能吸收该气体了,所以该气体密度比空气小,易溶于水.
故选C.
点评:易溶于水的气体可以用水来吸收,密度比空气大用向上排空气法收集,密度比空气小用向下排空气法收集,由图示可知空气从下端被排出,相当于向下排空气法收集.

练习册系列答案
相关题目
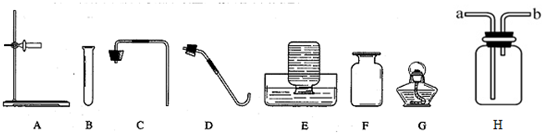
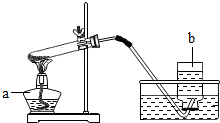 如图是某同学的实验室制氧气的装置图.
如图是某同学的实验室制氧气的装置图. 人类的生存离不开氧气.某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验:
人类的生存离不开氧气.某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验: