题目内容
 酸碱中和反应在实际生产生活中有着广泛的应用,如:改良酸性土壤,治疗胃酸过多等.小明同学在进行酸碱中和反应的实验时,,如图1向烧杯中的氢氧化钠溶液滴加盐酸一会,发现忘记了滴加指示剂,为了确定盐酸与氢氧化钠是否恰好完全反应,小明从烧杯中取少量反应后的溶液放在试管中,并向试管中滴加2滴无色酚酞,振荡,观察到酚酞试剂不变色.于是他得出“两种物质已恰好完全中和”的结论.
酸碱中和反应在实际生产生活中有着广泛的应用,如:改良酸性土壤,治疗胃酸过多等.小明同学在进行酸碱中和反应的实验时,,如图1向烧杯中的氢氧化钠溶液滴加盐酸一会,发现忘记了滴加指示剂,为了确定盐酸与氢氧化钠是否恰好完全反应,小明从烧杯中取少量反应后的溶液放在试管中,并向试管中滴加2滴无色酚酞,振荡,观察到酚酞试剂不变色.于是他得出“两种物质已恰好完全中和”的结论.(1)你认为他得出的结论
错误
错误
(填“正确或错误),理由是如果盐酸过量,滴入酚酞试液也不会变色
如果盐酸过量,滴入酚酞试液也不会变色
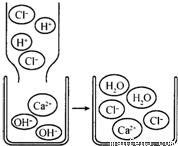
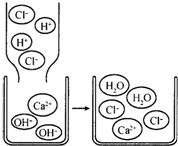
.(2)图2是小明同学绘制出的酸碱中和反应的微观示意图,该反应的化学方程式为
NaOH+HCl=NaCl+H2O
NaOH+HCl=NaCl+H2O
.(3)请你另设计实验,探究上述烧杯中的溶液是否恰好完全中和.
| 实验步骤 | 实验现象 | 结论 |
从烧杯中取少量反应后的溶液放在试管中,并向试管中滴加2滴紫色石蕊试液,振荡,观察 从烧杯中取少量反应后的溶液放在试管中,并向试管中滴加2滴紫色石蕊试液,振荡,观察 |
紫色石蕊试液变成红色 紫色石蕊试液变成红色 |
没有完全中和,盐酸过量 没有完全中和,盐酸过量 |
分析:(1)氢氧化钠和稀盐酸反应生成硫酸钠和水,酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应;
(2)根据反应物和生成物即可写出反应方程式;
(3)若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验即可.
(2)根据反应物和生成物即可写出反应方程式;
(3)若完全反应则溶液呈中性,若不是恰好完全反应,则呈酸性,因此可以从检验反应后的溶液中是否含酸着手设计实验即可.
解答:解:(1)向试管中滴加几滴无色酚酞试液不变色,因为酚酞试液在酸性和中性溶液中均为无色,故无法判断是否恰好完全反应.
故答案为:错误;如果盐酸过量,滴入酚酞试液也不会变色
(2)氢氧化钠和盐酸反应生成氯化钠和水;故答案为:NaOH+HCl=NaCl+H2O
(3)探究上述烧杯中的溶液是否恰好完全中和,可以从检验反应后的溶液中是否含酸着手设计实验,选择的试剂可以是紫色石蕊试液;
故答案为:(1)错误 如果盐酸过量,滴入酚酞试液也不会变色
(2)NaOH+HCl=NaCl+H2O
(3)
故答案为:错误;如果盐酸过量,滴入酚酞试液也不会变色
(2)氢氧化钠和盐酸反应生成氯化钠和水;故答案为:NaOH+HCl=NaCl+H2O
(3)探究上述烧杯中的溶液是否恰好完全中和,可以从检验反应后的溶液中是否含酸着手设计实验,选择的试剂可以是紫色石蕊试液;
故答案为:(1)错误 如果盐酸过量,滴入酚酞试液也不会变色
(2)NaOH+HCl=NaCl+H2O
(3)
| 实验步骤 | 实验现象 | 结论 |
| 从烧杯中取少量反应后的溶液放在试管中,并向试管中滴加2滴紫色石蕊试液,振荡,观察 | 紫色石蕊试液变成红色 | 没有完全中和,盐酸过量 |
点评:本题考查了酸碱指示剂的性质以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手;本题在检验溶液是否呈中性时也可以用碳酸钠等物质,当加入碳酸钠时,若有气泡产生的,则说明不是恰好完全反应;若没有气泡产生,则说明是完全反应.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目

 (2008?西城区二模)“世界是物质的,而物质是由粒子构成的”“化学变化的实质是粒子重新组合的过程”等都是化学学科中的重要观点.依据给定元素的化合价,从
(2008?西城区二模)“世界是物质的,而物质是由粒子构成的”“化学变化的实质是粒子重新组合的过程”等都是化学学科中的重要观点.依据给定元素的化合价,从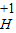 、
、 、
、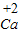 、
、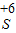 、
、 、
、 、
、 七种元素中任选一种或几种元素组成物质,回答下列问题.
七种元素中任选一种或几种元素组成物质,回答下列问题.