题目内容
【题目】中国制造业正在持续发展,公金是其中重要的金属材料。
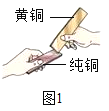
(1)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画(如图1所示),纯铜片上留下明显的划痕,说明______。
(2)黄铜渣中约含Zn7%、ZnO31%、Cu 50%、CuO5%,其余为杂质(杂质不溶于水、不参与反应)。处理黄铜渣可得到硫酸锌,主要流程如图2,操作中加热蒸发后冷却至原温度:
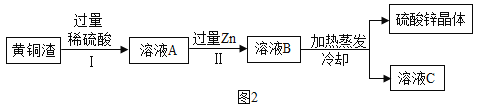
①溶液A中所含溶质为____________________;
②I、II 中的操作均包括________________;
③下列说法正确的是____________________。
A 溶液A中ZnSO4的质量大于CuSO4
B 溶液A的质量小于溶液B
C 溶液C中溶质的质量分数小于溶液B
(3)锌粉、铝粉、镁粉的混合物3.8g与一定质量的稀硫酸恰好完全反应,生成氢气0.2g,将反应后的溶液蒸发水分后得到固体混合物(不含结晶水)的质量为________g。
【答案】黄铜硬度比纯铜大 ZnSO4、CuSO4、H2SO4 过滤 AB 13.4
【解析】
(1)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画,纯铜片上留下明显的划痕,说明黄铜硬度比纯铜大。
(2)向黄铜渣中加入过量的稀硫酸,锌和氧化锌分别与稀硫酸反应生成硫酸锌,氧化铜与稀硫酸反应生成硫酸铜,故①溶液A中所含溶质为ZnSO4、CuSO4和过量的H2SO4。
②I、II 中的操作均包括是过滤,在I中通过过滤除去铜和不溶性杂质,在II 中通过过滤除去过量的锌。
③A、因为黄铜渣中Zn和ZnO的总含量大于CuO的含量,故溶液A中ZnSO4的质量大于CuSO4,A正确;
B、溶液A中含有ZnSO4、CuSO4、H2SO4,加入过量的锌,锌分别与CuSO4、H2SO4反应生成硫酸锌,锌的相对原子质量大于铜或氢的相对原子质量,故溶液A的质量小于溶液B,B正确;
C 溶液B通过蒸发溶剂冷却至原温度得到溶液C和硫酸锌晶体,则溶液C一定是该温度下的硫酸锌饱和溶液,而溶液B不是硫酸锌饱和溶液,故溶液C中溶质的质量分数可能大于溶液B,C不正确。故选AB。
(3)锌粉、铝粉、镁粉的混合物3.8g与一定质量的稀硫酸恰好完全反应,生成氢气0.2g。根据质量守恒定律,利用硫酸中氢离子与硫酸根离子的质量比,则参加反应的硫酸中硫酸根离子的质量为![]() 。反应后的溶液蒸发水分后得到固体混合物的质量等于原固体质量与参加反应中硫酸根离子的质量总和,则为
。反应后的溶液蒸发水分后得到固体混合物的质量等于原固体质量与参加反应中硫酸根离子的质量总和,则为![]() 。
。

【题目】图示所表示的各实验中相关量的变化关系,正确的是( )
A | B | C | D |
|
|
|
|
高温煅烧石灰石 (杂质不反应) | 氢氧化钠溶液中滴 加稀盐酸 | 接近饱和的硫酸铜溶液 中加入硫酸铜粉末 | 等质量、等浓度的稀盐酸中分别 放入足量的铁片和铝片 |
A.AB.BC.CD.D