题目内容
【题目】铁是生产、生活中应用很广泛的一种金属,下列是与铁的性质有关的部分实验图,请回答下列问题. 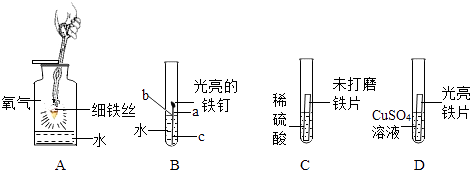
(1)A中细铁线燃烧生成黑色固体的化学式是 .
(2)B中铁钉最易生锈的部位是(填“a”、“b”或“c”).
(3)C中刚开始无气泡产生,溶液颜色逐渐由无色变为黄色,此时试管内发生反应的化学方程式是 .
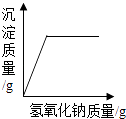
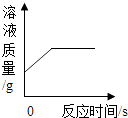
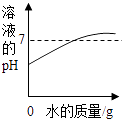
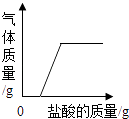
(4)D中反应一段时间后,试管内固体质量比反应前增大,据此推断,试管内溶液质量与反应前相比(填“增大”、“不变”或“减小”).
【答案】
(1)Fe3O4
(2)b
(3)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(4)减小
【解析】解:(1)铁丝的燃烧产物是四氧化三铁,四氧化三铁是黑色的固体,故答案为:Fe3O4;(2)铁生锈的条件:铁与水和氧气同时接触,所以因b处与水和氧气同时充分接触,所以最易生锈.
故答案为:b;(3)未打磨的铁片表面含有锈,锈与硫酸反应产生硫酸铁是黄色的溶液,故反应的方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(4)铁和硫酸铜反应产生硫酸亚铁和铜,试管内固体质量比反应前增大,根据质量守恒定律,试管内溶液质量与反应前相比减小;故答案为:减小.
(1)依据铁丝燃烧的实质书写方程式;(2)依据铁生锈的条件分析;(3)依据未打磨的铁片表面含有锈,结合实验的现象写出反应的方程式;(4)根据质量守恒定律分析溶液质量的变化.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】同学们在帮老师整理实验室时,发现石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【资料】①表是几种物质常温时的溶剂能力
②酚酞试剂遇碱性溶液变红色:石灰水溶液显碱性
OH﹣ | Cl﹣ | CO32﹣ | NO3﹣ | |
Ca2+ | 微 | 溶 | 不 | 溶 |
(1)对白色粉末成分的猜想和成因分析:
白色粉末的成分 | 形成的原因 |
可能是CaCO3 | 反应的化学方程式为: |
可能是Ca(OH)2 | 暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出 |
经过反复思考,同学们认为白色粉末还可能是二者的混合物.
(2)设计实验:甲同学取白色粉末装入试管中,加入少量水震荡,发现有白色固体不溶解,于是他得出粉末中一定有CaCO3 , 有人认为甲同学的结论不严密,理由是 . 为了得出较严密的结论,他们进行了如下实验,请完成下
(3)列实验报告:
实验步骤 | 可能观察到的现象 | 结论 |
取上述试管中的上次清夜,滴加1~2滴无色酚酞试液 | ||
向上述试管中的残留固体中加入稀盐酸 | 白色粉末(“有”或“无”)CaCO3 | |
由上述实验可知白色粉末的成分是: . | ||
(4)实际应用:向盛有碳酸钙粉末的试管中加入足量的稀盐酸,完全反应后共收集到4.4g二氧化碳气体,试计算反应消耗的碳酸钙的质量.