题目内容
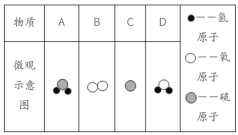
【题目】现有 A、B、C、D 四种物质,A 和 B 在一定条件下反应生成单质 C 和 D, 其微观模型如下表所示,则下列叙述错误的是( )
A. 物质 C 为硫单质
B. 该反应属于置换反应
C. 反应前后有元素的化合价发生改变
D. A、B、C、D 的化学计量数之比为 2:1:2:1
【答案】D
【解析】
由物质的微观示意图可知:A的化学式是H2S;B的化学式O2;C的化学式是S;D的化学式是H2O,则A、B、C、D四种物质中属于单质的有 2种,D物质的化学式为 H2O;化学方程式为:2H2S+O2![]() 2S+2H2O;A、物质C为硫单质,故正确;B、由反应的化学方程式可知:该反应是一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应,属于置换反应,故正确;C、由微粒的构成可知,该反应的生成物中有单质生成,反应物中有单质参加,所以,反应前后一定有元素的化合价发生改变;故正确;D、由反应的化学方程式可知:A、B、C、D的化学计量数之比为2:1:2:2,故错误。故选D。
2S+2H2O;A、物质C为硫单质,故正确;B、由反应的化学方程式可知:该反应是一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应,属于置换反应,故正确;C、由微粒的构成可知,该反应的生成物中有单质生成,反应物中有单质参加,所以,反应前后一定有元素的化合价发生改变;故正确;D、由反应的化学方程式可知:A、B、C、D的化学计量数之比为2:1:2:2,故错误。故选D。

【题目】某化学兴趣小组学习碱的性质后,到实验室做实验.小明将二氧化碳通入氢氧化钠溶液后无明显现象,然后向得到的溶液中滴加CaCl2溶液,产生白色沉淀;小杰做的实验和小明一样,但没有出现白色沉淀.他们为了查明原因,查阅资料:①CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CO2+H2O=2NaHCO3;②Ca(HCO3)2溶于水,溶液呈碱性;③CaCl2溶液呈中性:④Na2CO3、NaHCO3溶液都呈碱性,都能与酸反应;⑤铝、锌、铁、铜的盐溶液与NaHCO3溶液混合会产生沉淀.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3; 猜想②NaHCO3;
猜想③Na2CO3、NaOH; 猜想④_____________________.
【实验探究】
实验操作 | 实验现象 | 结论 |
(1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入____. | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式__________. |
(2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加_________. | 产生白色沉淀;______. | 猜想③成立 |
【继续探究】将4.0gNaOH固体溶解在100mL水中,然后通入4.0g二氧化碳气体,充分反应后,所得溶液的溶质是___________.