题目内容
【题目】(1)请根据如图回答问题。
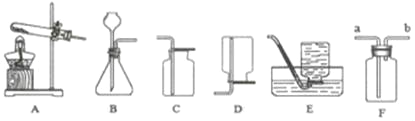
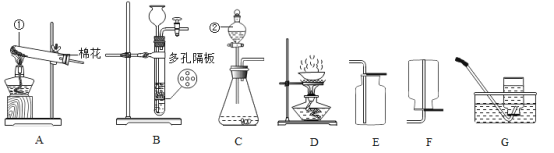
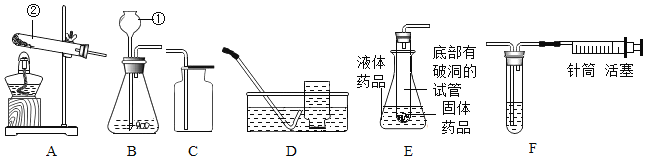
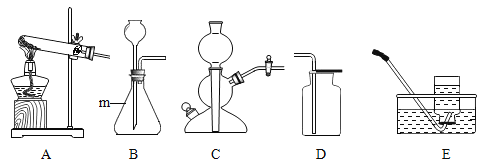
①图A中玻璃仪器的名称是_____(任写一种)
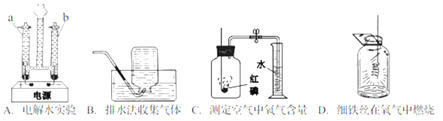
②若用过氧化氢溶液和二氧化锰的混合物制取并收集氧气,应选择上述装置中的_____,反应的化学方程式为_____。
③查阅资料:相同条件下,氨气的密度比空气小,且易溶于水:加热氯化铵和氢氧化钙固体混合物可制取氨气,根据所查资料,制取氨气应选择的发生装置是_____,收集装置是_____,小明同学欲用F装置收集氨气,氨气应从_____端进入(填“a“或“b”)。
(2)欲配制50g质量分数为10%的氯化钠的溶液,操作过程如图所示,看图回答下列问题:
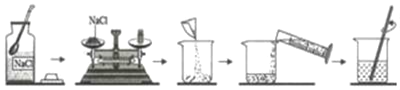
①称量时,应称取_____g食盐
②把水的密度近似地看作1g/mL,则须量取_____mL水;如果有10mL、50mL和100mL的量简,最好选取_____mL的量筒。
③实验中使用玻璃棒的目的是_____。
④如果所配得的溶液溶质的质量分数比大于10%,你认为可能的原因有_____。
A 量取水时俯视读数
B 所用氯化钠中含有杂质
C 称量时左托盘放砝码,右托盘放氯化钠(lg以下用游码)
D 未溶解充分就转移到试剂瓶中
【答案】试管(或酒精灯) BC或BE 2H2O2![]() 2H2O+O2↑ A D b 5 45 50 搅拌,加快氯化钠的溶解速率 A
2H2O+O2↑ A D b 5 45 50 搅拌,加快氯化钠的溶解速率 A
【解析】
(1)①图A中玻璃仪器有试管、酒精灯;故填:试管(或酒精灯);
②用过氧化氢溶液和二氧化锰的混合物制取氧气属于固液常温型,所以选择装置B来制取,氧气的密度比空气大,不易溶于水,所以可用向上排空气法或排水法来收集;过氧化氢在二氧化锰的催化作用下分解为水和氧气;故填:BC或BE;2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
③加热氯化铵和氢氧化钙固体混合物可制取氨气,该反应属于固体加热型,所以选择装置A来制取;相同条件下,氨气的密度比空气小,且易溶于水,所以用向下排空气法来收集;氨气的密度比空气小,所以用F装置收集氨气,氨气应从短管进入;故填:A;D;b;
(2)①配制50g质量分数为10%的氢化钠的溶液需要氯化钠的质量为:50g×10%=5g;故填:5;
②需要水的质量为:50g﹣5g=45g,水的体积为:45g÷1g/mL=45mL,选择50mL的量筒;故填:45;50;
③在溶解过程中玻璃棒的作用是搅拌,加快氯化钠的溶解速率;故填:搅拌,加快氯化钠的溶解速率;
④A、用量筒量取水时俯视读数,读数偏大但量取到的水正好偏小,溶质不变,溶剂少了,溶质质量分数偏大;
B、所用氯化钠中含有杂质则食盐变少,溶质质量分数偏小;
C、称量时左托盘放砝码,右托盘放氯化钠(1g以下用游码),实际质量是砝码减游码,溶质减小,溶质质量分数偏小;
D、未溶解充分就转移到试剂瓶中,则食盐变少,溶质质量分数偏小。
故填:A。