题目内容
【题目】了解物质的组成和结构,有助于认识物质的性质。
(1)下图表示核电荷数为11~17的元素最高和最低化合价。
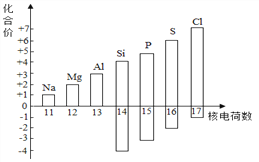
①从图中可以看出,氯元素的最高正价是__________。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为__________。
③写出图中元素的化合价随着核电荷数递增的一条变化规律_____________________。
④从微观的角度来看,图中元素的原子在构成上的共同特征是_____________________。
(2)在金属活动性顺序表里,通常排在前面的金属更易失去电子。回答以下问题:
①某金属原子的结构示意图为![]() ,则最外层电子数x=_____________;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为_______________。
,则最外层电子数x=_____________;若最外层电子失去,达到相对稳定结构,该带电粒子的符号为_______________。
②我国古代发明了“曾青(即硫酸铜)得铁化为铜”的湿法炼铜法,请用化学方程式表示反应原理__________________;反反应中,更易失去电子的金属是________。
【答案】 +7 8 最高正价依次递增 电子层数均为三层 3 Al3+ Fe+CuSO4=FeSO4+Cu Fe
【解析】(1)①从图中可以看出,氯元素的最高正价是+7价;②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为=|+7|+|-1|=8;③根据表格提供的信息可以看出,同一行元素化合价具有的规律是:从左到右元素的最高正化合价逐渐从+1升高到+7;④核电荷数为11~17的元素都在元素周期表的第三周期,从微观的角度来看,图中元素的原子在构成上的共同特征是:电子层数均为三层;(2)①最外层电子数x=3,该带电粒子的符号为该带电粒子的符号为Al3+;②湿法炼铜法,化学方程式表示:Fe+CuSO4=FeSO4+Cu;此反应说明铁比铜活泼,铁更易失去电子。