题目内容
【题目】某兴趣小组以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究.如图1所示,小组同学向氢氧化钠溶液加入稀硫酸.一会儿发现忘记了滴加指示剂,因此,他们停止滴加稀硫酸,并对试管内稀硫酸与氢氧化钠溶液是否发生了反应进行探究. 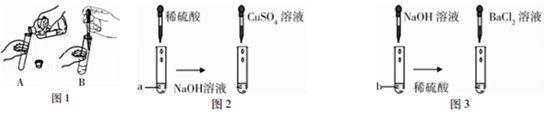
(1)图1实验操作:A是取用氢氧化钠溶液的操作,B是向氢氧化钠溶液中滴加稀硫酸的示意图. ①请指出A中两处的错误:、 .
②同学认为按照B图所示操作,可以令液体沿试管内壁流下避免迸溅,又可以避免因拿滴管的手抖动使得稀硫酸滴在持试管的手上.但实验室禁止按照B图所示操作,请你推测B图所示操作可能导致的不良后果: .
(2)小组同学设计了以下实验方案:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
(3)写出该反应的化学方程式: .
(4)同学们经过讨论一致认为,不用上述方法,用其他试剂也可以证明稀硫酸与氢氧化钠溶液能发生反应.于是分成甲、乙两组继续试验. 甲组实验:探究CuSO4溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
【实验操作及现象】
如图2,向试管a中滴加足量稀硫酸时无明显现象,再滴加CuSO4溶液时没有出现蓝色沉淀.
【实验结论1】
通过以上实验操作及现象,你认为用CuSO4溶液(填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应.
乙组实验:探究BaCl2溶液是否可以证明稀硫酸与氢氧化钠溶液发生反应.
【实验操作及现象】
如图3,向试管b中滴加足量NaOH溶液时无明显现象,再滴加BaCl2溶液时出现白色沉淀.
【实验结论2】
通过以上实验操作及现象,你认为用BaCl2溶液(填“可以”或“不可以”)证明稀硫酸与氢氧化钠溶液能发生反应.理由是 .
【答案】
(1)瓶塞正放;标签没有向着手心;试剂交叉污染
(2)<
(3)2NaOH+H2SO4═Na2SO4+2H2O
(4)可以;不可以;硫酸能和氯化钡反应生成硫酸钡沉淀和盐酸
【解析】解:(1)①A中两处的错误是:瓶塞正放,并且没有向着手心. 故填:瓶塞正放;并且没有向着手心.
②推测B图所示操作可能导致的不良后果是试剂交叉污染.
故填:试剂交叉污染.(2)实验方案如下表所示:
实验步骤 | 实验现象 | 实验结论 |
在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量反应后的溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡比较,读溶液的pH | pH<7 | 稀硫酸与氢氧化钠溶液发生了反应,且稀硫酸过量了. |
;(3)氢氧化钠和稀硫酸反应生成硫酸钠和水,该反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O.
故填:2NaOH+H2SO4═Na2SO4+2H2O.(4)【实验结论1】通过以上实验操作及现象,用CuSO4溶液可以证明稀硫酸与氢氧化钠溶液能发生反应,这是因为如果氢氧化钠没有和硫酸反应,则能和硫酸铜反应生成蓝色沉淀.
故填:可以.
【实验结论2】
通过以上实验操作及现象,用BaCl2溶液不可以证明稀硫酸与氢氧化钠溶液能发生反应.理由是硫酸能和氯化钡反应生成硫酸钡沉淀和盐酸.
故填:硫酸能和氯化钡反应生成硫酸钡沉淀和盐酸.
【考点精析】通过灵活运用中和反应及其应用和书写化学方程式、文字表达式、电离方程式,掌握中和反应:酸与碱作用生成盐和水的反应;注意:a、配平 b、条件 c、箭号即可以解答此题.

 阅读快车系列答案
阅读快车系列答案