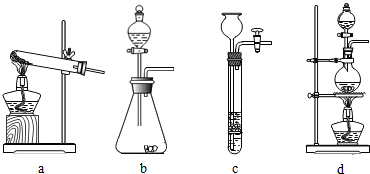
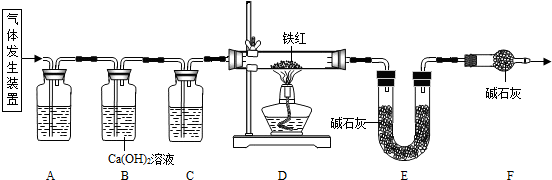
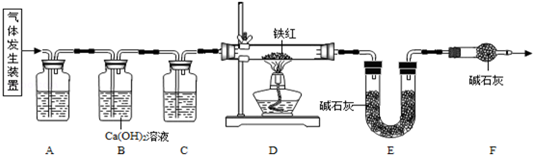
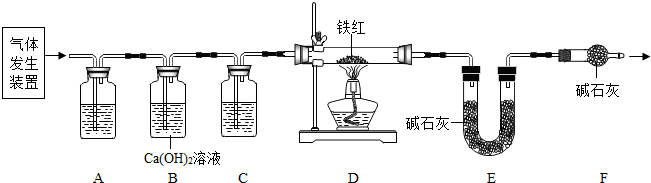
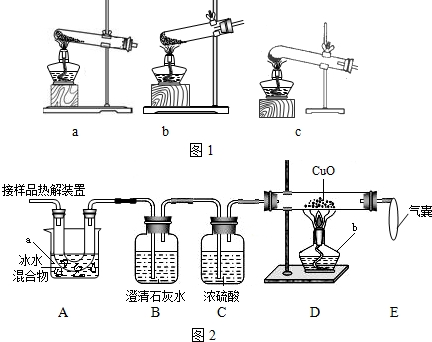
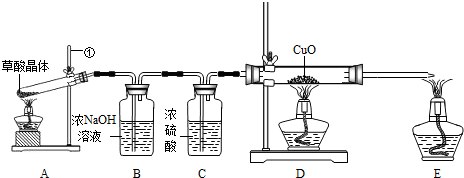
��Ŀ����
���ᾧ�壨H2C2O4��2H2O���۵�ϵͣ����Ȼ��ۻ��������ͷֽ⡣���ᣨH2C2O4�����Ȼ�ֽ⣬�����������Ƶķ�ӦΪ��H2C2O4+Ca(OH)2==CaC2O4��(��ɫ)+2H2O��
�ס�����ͬѧ�Բ������ȷֽ�IJ���������̽����
��1����������裺
��һ�֣�����ֽ�����CO2��H2��
�ڶ��֣�����ֽ�����CO2��CO��H2O��
�����֣�����ֽ⣺H2C2O4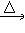 CO2��+H2O��δ��ƽ����
CO2��+H2O��δ��ƽ����
��ͬѧ�������ϾͿ��жϵ����ּ��費��������ʦҲ��Ϊ��һ�ж�����ȷ�ģ���ͬѧ�жϵ�����������________________________��
��2�������ʵ�飺�ס�����ͬѧ�ֱ��������ͼ��ʾ��A��B����ʵ��װ�ã�ͼ������̨��ȥ����
�ס�����ͬѧ�Բ������ȷֽ�IJ���������̽����
��1����������裺
��һ�֣�����ֽ�����CO2��H2��
�ڶ��֣�����ֽ�����CO2��CO��H2O��
�����֣�����ֽ⣺H2C2O4
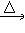 CO2��+H2O��δ��ƽ����
CO2��+H2O��δ��ƽ������ͬѧ�������ϾͿ��жϵ����ּ��費��������ʦҲ��Ϊ��һ�ж�����ȷ�ģ���ͬѧ�жϵ�����������________________________��
��2�������ʵ�飺�ס�����ͬѧ�ֱ��������ͼ��ʾ��A��B����ʵ��װ�ã�ͼ������̨��ȥ����

�ټ�ͬѧ��Aװ��ʵ�飬�۲쵽����ʯ��ˮ����ǣ���Ϊ���������ɲ��ᾧ�����ȷֽ������CO2�����£����ж�_______������ܡ������ܡ�����
����ͬѧ��Bװ��ͼ�����ڵ�����δ�����������������������ֱ�ӻ���ͼ�ϻ����ϣ�����ͬѧ��Bװ��ʵ�飬������ˮ����ͭ�ɰױ�����ϴ��ƿ����Һ����ǡ��ڼ���ܿڵ�ȼʣ�����壬�����Ϸ���һ��___________�ձ����а�ɫ�������ɣ�֤����������____________����һ���ɡ����ձ����ڻ����Ϸ����ڱ�������֤����������H2��
��3��������˼����
�ٲ������ȷֽ�Ļ�ѧ����ʽΪ��______________________��
����ʡ��Bװ�÷����ڵ�����������װ��Ҳ��֤����������CO2������ÿ������Ӧ��ȫ���������ǣ�___________________________________________��
��1����������ƽ���䲻ƽ���������غ㶨�ɻ�ֻ�л��ϼ۵����ߣ����ϼ۵Ľ���
��2���ٲ�����
������ͼ �����ܲ�����Һ���²����֣���������Ҫ��
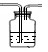
�ڱڸ��г���ʯ��ˮ�����������𰸾����֣���CO
��3����H2C2O4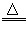 CO2����CO����H2O��
CO2����CO����H2O��
�� ����ʵ��ǰ��ʢ�м�ʯ�ҵĸ���ܵ���������˼����ı��������֣�
��2���ٲ�����
������ͼ �����ܲ�����Һ���²����֣���������Ҫ��

�ڱڸ��г���ʯ��ˮ�����������𰸾����֣���CO
��3����H2C2O4
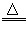 CO2����CO����H2O��
CO2����CO����H2O���� ����ʵ��ǰ��ʢ�м�ʯ�ҵĸ���ܵ���������˼����ı��������֣�

��ϰ��ϵ�д�
 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
�����Ŀ