题目内容
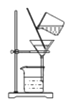
【题目】20℃时,向 100g 水中分别加入等质量的甲、乙两种固体(如图 1)。升温到 50℃时溶液如图 2 所示。请结合溶解度曲线判断,下列说法中错误的是

A.图 3 中 M 表示甲物质的溶解度曲线
B.图 2 中的甲溶液降温,溶质质量分数一定减小
C.图 1 中乙形成的可能是饱和溶液
D.图 1、图 2 中乙溶液的溶质质量分数相同
【答案】B
【解析】
A.20℃时,向100g水中分别加入等质量的甲、乙,甲烧杯底部有固体剩余,乙烧杯底部没有固体剩余,所以20℃时,甲物质的溶解度小于乙物质的溶解度,所以M表示甲物质的溶解度曲线,N表示乙物质的溶解度曲线,故A正确;
B.图2中的甲溶液降温,如果甲恰好饱和,则降温后,有晶体析出,溶质质量分数减小,如果是不饱和溶液,降温后,溶质质量分数不一定减小,还可能不变,故B错误;
C.图1中乙烧杯底部没有固体剩余,乙可能恰好饱和,也可能不饱和,所以形成的可能是饱和溶液,故C正确;
D.图1、图2乙溶液中的溶质和溶剂不变,所以乙溶液的溶质质量分数相同,故D正确。
答案选B。

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
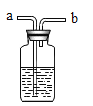
一课一练课时达标系列答案【题目】化学兴趣小组在解老师的带领下探究“饱和氢氧化钙溶液导电性"实验时(如图),发现了一个意外现象:两根石墨电极两端产生氢气、氧气以外,饱和澄清石灰水中出现了白色浑浊。为此,小组同学展开了如下探究。
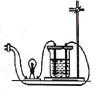
[提出问题]为什么出现白色浑浊?
[猜想与假设]
甲:可能是饱和溶液电解时________减少,氢氧化钙固体析出导致的浑浊;
乙:可能是饱和溶液通电时温度升高,氢氧化钙固体析出导致的浑浊;
丙:可能是电解过程中产生的___________与饱和石灰水反应导致的浑浊。
[进行实验]小组同学分别设计了如下实验方案验证。
实验步骤 | 实验现象 | 实验结论 | |
甲 | 将90mL相同浓度的饱和澄清石灰水中加入10mL蒸馏水,在相同的电压下再次进行电解实验,观察现象 | _______________。 | 甲同学猜想不正确 |
乙 | 取_____________于烧杯中,加热至电解实验中上升的相同温度,观察现象 | 溶液不变浑浊 | 乙同学猜想____。 |
丙 | 向电解得到浑浊液体中加入足量的稀盐酸,观察现象 | 浑浊消失,有气泡产生。该反应化学方程式为____________。 | 丙同学猜想正确 |
[拓展延伸][注意:若答对以下问题可奖励4分,化学试卷总分不超过60]
为进一步研究丙同学实验后废液成分性质,丁同学取一定质量的废液,逐滴加入溶质质量分数为10.6%的Na2CO3溶液,实验过程中加入Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示:
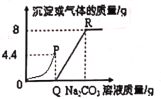
①P点时的溶液中的溶质是____________________(写名称);
②R点对应横坐标的数值为______________________;
③Q至R段表示_________________________________的过程。