��Ŀ����
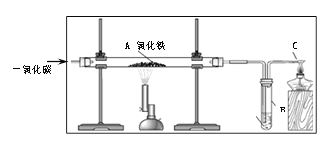
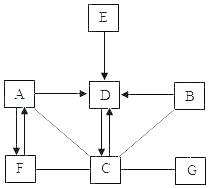
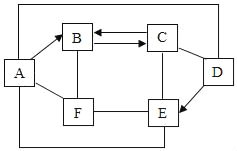
����Ŀ����ú�������ļ�����չ����200����ʷ��ijʵ���������һ��ú���⼼��������������ͼ��ʾ��
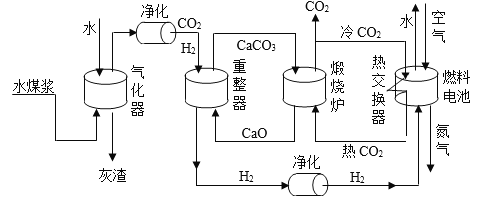
(1)ˮú������ú(��Ҫ��̼)��ˮ��϶��ɣ�������������ת��ΪCO2��H2�����������з�����������Ӧ(��Ӧ������ʡ��)����C + H2O = CO + H2 ���� + �� = CO2 + H2
�ٵĻ�����Ӧ������________���ڵĻ�ѧ����ʽ��________��
(2)��������������______��
(3)ȼ�ϵ������ķ�ӦΪ��2H2+O2 = 2H2O��Ϊ��ά����ص�������������Ҫ�����ŷ������ɵ�ˮ��100kg����ͨ��ȼ�ϵ�أ������Ͽ�����ˮ_______kg��
���𰸡��û���Ӧ CO + H2O = CO2 + H2����CO2��H2(��ȥ�����л��еĶ�����̼)900
��������
(1)�ɢ�C+H2O=CO+H2��֪���÷�Ӧ��һ�ֵ��ʺ�һ�ֻ����ﷴӦ��������һ��һ�ֵ��ʺ���һ�ֻ���������û���Ӧ�����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�ӵ�������������䣬�ڵĻ�ѧ����ʽ�ǣ�CO+H2O=CO2+H2��(2)�������������Ƿ���CO2��H2����ȥ�����л��еĶ�����̼����(3)�������Ͽ�����ˮ������Ϊx��
2H2+O2=2H2O
4 36
100kg x
![]()
x=900kg��

��ϰ��ϵ�д�
�����Ŀ