题目内容
【题目】下列是人类发现二氧化碳历程中的部分资料。
(资料一)1630年,海尔蒙特发现在一些洞穴处,有一种能使燃着的蜡烛熄灭的气体,后来被证实是CO2。
(资料二)1754年,布莱克将石灰石煅烧首次制得CO2。
(资料三)1766年,卡文迪许通过实验测得,室温下1体积水大约能溶解1体积二氧化碳气体。
(资料四)1767年,卡文迪许发表论文介绍了他做的一个实验:①向澄清的石灰水中通入二氧化碳气体,开始时产生白色沉淀,②继续通入二氧化碳气体后,沉淀溶解,溶液再次变的澄清;③他将澄清这溶液煮沸,溶液变浑浊并放出气体。
(1)根据海尔蒙特的发现,可推测二氧化碳的一个重要用途是灭火,这是利用了二氧化碳的_______性质。
(2)布莱克实验中,若要检验石灰石是否完全分解,方法是_______________。
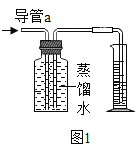
(3)如图1,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入250毫升CO2,如果卡文迪许的结论是正确的,则现象是___________________。
(4)写出(资料四)中卡文迪许介绍的实验中有关反应的化学方程式:
①__________________________。
③__________________________ 。
(5)某兴趣小组的同学在实验室用如图2仪器制取气体
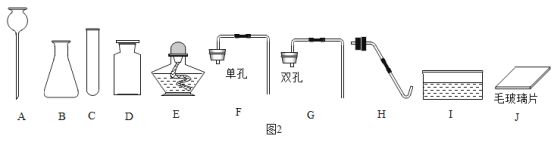
①仪器B的名称是______________。
②用图2仪器制备并收集二氧化碳,则应选择的仪器组合是__________,发生反应的化学方程式为___,若选用氯酸钾制取氧气,则除上述给出仪器外,还必须增加的实验仪器是____________。
③SO2与CO2的化学性质有相似之处。实验室可用Na2SO3与70%的硫酸在常温下反应制备SO2,尾气必须要进行处理,其原因是__________________,若用氢氧化钠溶液吸收二氧化硫,反应的化学方程式为_________________________。
【答案】二氧化碳不可燃不助燃且密度比空气大 向其中加入足量稀盐酸,若有气泡产生说明石灰石没有完全分解 广口瓶内的水会有50mL沿导管进入量筒内 ![]()
![]() 锥形瓶 BFDJ 或ABGDJ CaCO3+ 2HCl = CaCl2 + H2O + CO2↑ 铁架台 二氧化硫有毒,会污染空气 2NaOH + SO2 = Na2SO3 + H2O
锥形瓶 BFDJ 或ABGDJ CaCO3+ 2HCl = CaCl2 + H2O + CO2↑ 铁架台 二氧化硫有毒,会污染空气 2NaOH + SO2 = Na2SO3 + H2O
【解析】
(1)二氧化碳能灭火,这是利用了二氧化碳不可燃不助燃且密度比空气大。
(2)如果石灰石没有完全分解,则生石灰中含有碳酸钙,检验石灰石是否完全分解方法是向其中加入足量稀盐酸,若有气泡产生说明石灰石没有完全分解。
(3)根据室温下1体积水大约能溶解1体积二氧化碳气体,在室温下将容积为200毫升的广口瓶注满蒸馏水,通过导管a缓慢通入250毫升CO2,则有50毫升CO2不能溶解于水中,现象是广口瓶内的水会有50mL沿导管进入量筒内。
(4)实验中有关反应的化学方程式:
①是向澄清的石灰水中通入二氧化碳气体,产生白色沉淀,反应方程式为![]() 。
。
③将澄清这溶液煮沸,碳酸氢钙分解,溶液变浑浊并放出气体,反应方程式为![]() 。
。
(5)①仪器B是锥形瓶。
②制备二氧化碳是用石灰石和稀盐酸反应,反应原理是固体液体不需加热,发生装置可选择ABG,二氧化碳的密度比空气大且能溶于水,收集二氧化碳可选用向上排空气法,故制备并收集二氧化碳应选择的仪器组合是ABGDJ;反应的化学方程式为CaCO3+ 2HCl = CaCl2 + H2O + CO2↑,选用氯酸钾制取氧气,则除上述给出仪器外,还必须增加的实验仪器是铁架台,因为该反应需要加热,用铁架台固定发生装置。
③实验室可用Na2SO3与70%的硫酸在常温下反应制备SO2,尾气必须要进行处理,其原因是二氧化硫有毒,会污染空气;用氢氧化钠溶液吸收二氧化硫,生成亚硫酸钠和水,反应的化学方程式为2NaOH + SO2 = Na2SO3 + H2O。

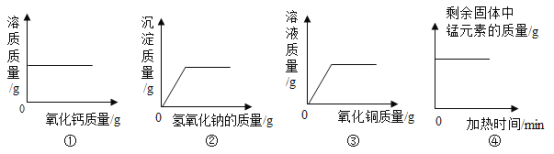
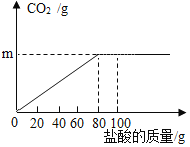
【题目】钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像。请根据有关信息回答问题
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | 30 | 25 | 20 | a |
(1)求碳酸钙中各元素的质量比Ca:C:O=___________。(化成最简整数比)
(2)a的数值为_______,该品牌补钙药剂中CaCO3的质量分数是_______
(3)求该盐酸中溶质的质量分数_______(写出计算过程,计算结果保留一位小数)。
【题目】几年前在浙江发生一起严重火灾,一辆载满20t电石的挂车燃起熊熊大火并伴有大量黑烟。事故路面上洒落了五六百米燃着的“石头”。这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼。这则新闻使大家对电石的化学性质产生了浓厚的兴趣,请你与他们一起完成下列探究活动。
(查阅资料)
电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体。常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟。
(猜想与假设)
电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙。大家做出以上推断的理由是_________。大家讨论后一致认为该气体不可能是氧气,原因是_________________,白色固体不可能是氧化钙,原因是(用化学方程式表示) ____________。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
(1)取适量电石加水反应,收集生成的气体,验纯后点燃。 | 气体燃烧,产生黄色火焰并伴有浓烈黑烟。 | 电石与水反应产生的气体是_________ |
(2)取适量反应后生成的固体于试管中,滴加过量稀盐酸。 | 固体溶解, _________. | 电石与水反应产生的固体不是碳酸钙 |
(3)取适量反应后生成的固体于试管中加水,向上层清液中滴加 2~3滴_________。 | __________________ | 电石与水反应产生的固体是氢氧化钙 |
(反思交流)载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是_________(填“吸热”或“放热”)反应。
【题目】实验室常用加热氯酸钾和二氧化锰混合物的方法制取氧气,请回答下列问题:
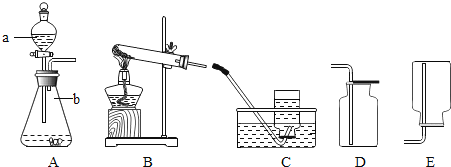
(1)反应的化学方程式为________.
(2)写出下列编号仪器的名称![]() ________
________![]() ________.
________.
(3)用所给仪器组装用上述反应制氧气的装置,你选择的发生装置为________,![]() 装置试管口要略向下倾斜的原因是________;收集装置为________.
装置试管口要略向下倾斜的原因是________;收集装置为________.
上述装置选择的依据是________(填字母).
![]() 属于固固型加热的反应
属于固固型加热的反应 ![]() 属于固液型不加热的反应
属于固液型不加热的反应
![]() 制取的气体密度比空气大
制取的气体密度比空气大 ![]() 制取的气体难溶于水
制取的气体难溶于水
(4)若用图⑥装置进行“排空气法”收集制取的![]() ,请把图中的“导气管”补画完整_____.
,请把图中的“导气管”补画完整_____.
(5)有几位同学一起探究:氯酸钾和二氧化锰混合为多少比例时,产生氧气的速度最快.实验时用秒表记录时间,计时从加热到收集满一瓶氧气为准,实验所采用的装置是将![]() 和________组合起来.下表为二氧化锰与氯酸钾不同质量比时,制取氧气的速度比较
和________组合起来.下表为二氧化锰与氯酸钾不同质量比时,制取氧气的速度比较
实验序号 | 二氧化锰与氯酸钾的质量比 | 用时(秒) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
从实验序号![]() 和
和![]() 数据可以看出,实验序号________(填
数据可以看出,实验序号________(填![]() 或
或![]() )反应速度最快.通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”)________越多越好.
)反应速度最快.通过分析可知,在化学反应中催化剂的用量(填“是”或“不是”)________越多越好.
(6)若在反应后的残余物中提纯![]() ,需进行以下操作,请把空缺处填上:_____、_____
,需进行以下操作,请把空缺处填上:_____、_____
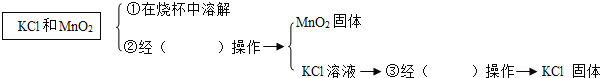
在①、②、③的操作中均用到的仪器是________.