题目内容
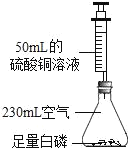
【题目】王老师指导化学兴趣小组的同学,设计了“测量空气中氧气体积分数”实验的新装置(见图),并进行了以下探究活动,请你一同参与。
(小资料)
(1)白磷着火点约为40℃,易燃烧,且耗氧彻底;
(2)硫酸铜溶液能与白磷反应,从而化解白磷的毒性。
(实验探究)
(1)在确保装置不漏气时,按图装入药品、连好仪器。
(2)将锥形瓶底部放入热水中,白磷很快被引燃。请写出白磷燃烧的化学方程式_____。
(3)燃烧结束,等到锥形瓶冷却到室温后,把注射器针头穿透橡皮塞,此时注射器里的硫酸铜溶液会_____;如实验比较成功,测得氧气的体积分数约是_____,最终注射器里的液面约停留在_____mL刻度处。
(反思与评价)
(1)实验结束、振荡锥形瓶,硫酸铜溶液能与剩余的白磷发生反应,化学方程式为:11Px+60CuSO4+96H2O=20Cu3P↓+24H3P04+60H2SO4,则白磷化学式中的x=_____。
(2)足量的白磷在锥形瓶中未能全部燃烧,这说明瓶内剩余气体_____(填“支持”或“不支持”)燃烧。
(3)此改进装置与课本上“测量空气中氧气体积分数”实验装置相比,有不少的优点,请你写出一条:_____。
【答案】4P+5O2=2P2O5 自动喷入锥形瓶内 ![]() 4 4 不支持 不污染环境、误差小
4 4 不支持 不污染环境、误差小
【解析】
实验探究:
(2)锥形瓶底部放入热水中,白磷由于着火点较低,能够自燃,生成五氧化二磷,此处方程式的条件不能是点燃,化学反应方程式为4P+5O2=2P2O5;
(3)燃烧结束,等到锥形瓶冷却到室温,因为锥形瓶内压强减少,硫酸铜溶液会自动喷入锥形瓶内,如实验比较成功,因为空气中氧气与站空气体积的![]() ,所以进入的硫酸铜溶液应该是230ml×
,所以进入的硫酸铜溶液应该是230ml×![]() =46mL,则最终注射器里的液面约停留在4mL刻度处;
=46mL,则最终注射器里的液面约停留在4mL刻度处;
反思与评价:
(1)依据质量守恒定律中反应前后原子的个数不变可知:当X=4时反应前后各原子的个数均相等,符合质量守恒定律。
(2)足量的白磷在锥形瓶中未能全部燃烧,这说明瓶内剩余气体不燃烧也不支持燃烧;
(3)优点是:不污染环境、误差小等;

【题目】小明在学习金属活动性顺序后,知道钾、钙、钠的金属活动性特别强,能与水反应生成碱和氢气。他思考镁紧排在钠后面,那么它是否也能与水反应呢?
【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂。实验过程和现象如图:

【反思与总结】
(1)小明得出的实验结论是________________________________。
(2)小明发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了。
猜想 | 验证方案 |
可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱 | 将褪色的溶液________,如果溶液变红,说明小明的猜想正确 |
小明通过实验证明了自己的猜想是正确的。
(3)一段时间后,小明观察到镁条在热水中无现象,但当他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是________________________________________________________________________。