题目内容
【题目】某金属冶炼厂的管道烟泥中含有Cu、Zn及炭黑,现欲回收铜和锌,主要流程如图所示:
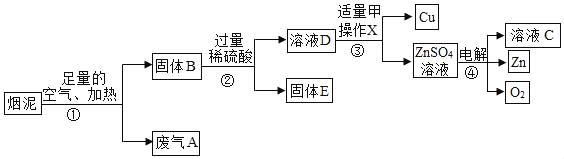
(1)步骤①产生的废气A中,一定含有的气体是_____。
(2)溶液D中一定含有的溶质是_____。
(3)步骤③中发生反应的化学方程式是_____(任写一个)。操作X的名称是_____;其所需玻璃仪器除漏斗、玻璃棒外,还有_____。
(4)步骤④中参加反应的物质为ZnSO4和_____(填化学式)。
(5)有人认为若步骤①中空气不足量,会导致锌的回收率降低,你认为是否正确?_____(填“正确”或“不正确”),理由是_____。
【答案】SO2 CuSO4、ZnSO4、H2SO4 Zn+H2SO4═ZnSO4+H2↑或Zn+CuSO4=ZnSO4+Cu 过滤 烧杯 H2O 不正确 不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收
【解析】
根据烟泥中含有硫的单质,所以加热后会生成有毒气体二氧化硫进行分析;通过生成物的分析可以看出甲是锌反应时会置换出铜,并消耗溶液中的剩余硫酸;过滤是把固体和液体分开的操作;空气量不足不会影响锌的回收,因为不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收。
(1)烟泥中存在单质硫,在空气中加热时会产生二氧化硫,二氧化硫是常见的空气污染物;故填:SO2
(2)经过操作X得到了铜和硫酸锌,故D中一定含有硫酸铜和硫酸锌,由于硫酸是过量的,一定含有硫酸,故填:CuSO4、ZnSO4、H2SO4
(3)③中加入的甲是锌,与硫酸反应生成硫酸锌,与硫酸铜反应生成硫酸锌和铜,X是过滤操作,需要的玻璃仪器有烧杯、漏斗和玻璃棒,故填:Zn+H2SO4═ZnSO4+H2↑或Zn+CuSO4=ZnSO4+Cu;过滤;烧杯
(4)电解硫酸锌溶液得到的是锌、氧气以及溶液C,故水也参加了反应,故填:H2O
(5)空气量不足不会影响锌的回收,因为不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收,故填:不正确;不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收

【题目】张玲同学为测定汉白玉中碳酸钙的质量分数,称取5.55g研碎的汉白玉粉末进行四次高温加热、冷却、称量剩余固体的重复操作。记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | 4.25 | 3.95 | 3.35 | 3.35 |
请计算:
(1)完全反应后产生的二氧化碳质量_____;
(2)汉白玉中碳酸钙的质量分数________。