题目内容
【题目】今年的实验测试考核时,萧红中学某小组同学抽到的题目是区分碳酸钠与氢氧化钠溶液,提供的药品有:酚酞溶液、稀硫酸、氯化钡溶液、氢氧化钡溶液、稀硝酸。
[实验探究]分别取两种溶液样品,标注为1号和2号,再分别加入一定量的稀硫酸,观察到1号样品无明显现象,2号样品中产生气泡;
[实验结论]产生气泡的方程式为________;
实验结束,他们将两支试管里的废液倒入废液缸时没有看到任何现象,同学们利用所给的药品对废液缸中的成分继续探究。
[提出问题]废液中除含有Na2SO4外,还可能含有哪些溶质? (用化学式填写)
[猜想与假设]小萧:NaOH;小红:Na2CO3;小辉:NaOH、Na2CO3;小煌:_______;
[实验探究]小辉同学为了验证自己的猜想,做了如下实验:

(解释与结论]小辉观察到步骤一中产生了白色沉淀,步骤二中上层清液变红,所以得出结论:自己猜想正确。
[评价与交流]请你评价小辉同学的结论:__________。
同学们经讨论后一致认为:小辉同学若将步骤一中的 Ba( OH)2溶液换成另一种试剂,步骤二后过滤,再向滤渣中加入________,就可以通过明显的现象验证自己的猜想。若小辉同学的猜想正确,则应观察到的滤渣中的现象是_________。
[归纳与总结]通过上述实验小煌能够总结出:如果被验证的溶液中两种溶质成分化学性质有相似点时,则应先通过分析两种溶质的_______,分别加入不同的试剂通过_____分別证明。
【答案】![]() H2SO4 小辉的结论不正确,硫酸钠能与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠,也有沉淀产生,生成的氢氧化钠和过量的氢氧化钡也能使无色酚酞试液变红 稀盐酸或稀硝酸 滤渣逐渐溶解,有气泡产生; 性质不同点 验证并除去一种溶质,然后再验证另一种溶质的存在
H2SO4 小辉的结论不正确,硫酸钠能与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠,也有沉淀产生,生成的氢氧化钠和过量的氢氧化钡也能使无色酚酞试液变红 稀盐酸或稀硝酸 滤渣逐渐溶解,有气泡产生; 性质不同点 验证并除去一种溶质,然后再验证另一种溶质的存在
【解析】
实验结论:产生气泡是因为碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳和水,该反应的化学方程式为:![]() ;
;
猜想与假设:两支试管中发生的反应分别为:氢氧化钠与稀硫酸反应生成硫酸钠和水,碳酸钠和稀硫酸反应生成硫酸钠、二氧化碳和水,实验结束,将两支试管里的废液倒入废液缸时没有看到任何现象,可能是碳酸钠过量,或者氢氧化钠过量,或者氢氧化钠与碳酸钠都过量,或者稀硫酸过量,故小煌:H2SO4;
评价与交流:小辉的结论不正确,硫酸钠能与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠,也有沉淀产生,生成的氢氧化钠和过量的氢氧化钡也能使无色酚酞试液变红,步骤一中产生了白色沉淀,步骤二中上层清液变红,不能说明溶质中含有碳酸钠和氢氧化钠;
小辉同学可将步骤一中的 Ba( OH)2溶液换成氯化钡,氯化钡与碳酸钠反应生成碳酸钡和氯化钠,步骤二后过滤,再向滤渣中加入稀盐酸,碳酸钡与稀盐酸反应生成氯化钡、二氧化碳和水,有气泡产生,若小辉同学的猜想正确,则应观察到的滤渣中的现象是:滤渣逐渐溶解,有气泡产生;

【题目】(1)小琪等几位同学准备进行鉴别澄清石灰水和氢氧化钠溶液的实验探究,请你参与:
(提出问题)如何鉴别这两种无色溶液?
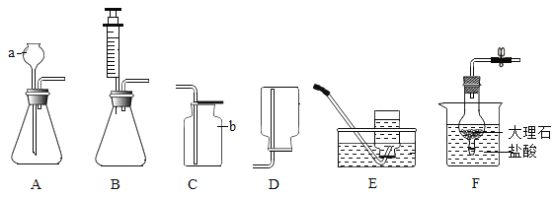
(实验方案)他们进行了如图所示的实验

请你回答下列问题:
①四组实验中不能达到实验目的是___________(填字母);
②C组实验中反应的化学方程式为________________________;
③D组实验中变浑浊的原溶液是_______________。
(继续探究)实验结束后,小琪同学将A、B、C、D四组试管中的物质全部倒入同一个干净的烧杯中,充分反应后,得到无色澄清透明的溶液,对该溶液的成分又进行了探究.
(提出问题)该溶液中除水、酚酞外还含有哪些物质?
(查阅资料)氯化钙溶液呈中性.
(猜想与假设)
Ⅰ._______________
Ⅱ.NaCl、CaCl2、HCl
Ⅲ.NaCl、CaCl2、NaOH
(反思与拓展)①上述猜想与假设中只有一个不成立,它是_____(填序号),理由是________。
②根据所学化学知识,验证烧杯内溶液中可能有的物质是否存在,下列哪些物质单独使用不能完成该实验___________(填字母)
a pH试纸 b 硝酸银溶液 c 紫色石蕊试液 d 铜 e 足量氢氧化钠溶液.
(2)葡萄糖是生命体所需能量的主要来源。
(提出问题)葡萄糖的燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
(设计实验)为了确定葡萄糖的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略)。
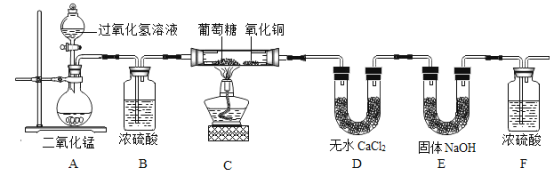
①装置A中发生反应的化学方程式是__________________________;
②装置B中浓硫酸的作用是_________________________。
③装置C处氧化铜的作用是_________________________。
(方案评价)
①用充有空气的储气球代替装置A,是否更有利于实验的进行?_____(填“是”或“否”)原因是______________________。
②装置C处葡萄糖燃烧的设计特点是_________________(至少一条)。
(数据处理)下表是同学们填写的实验报告,请你帮助完成。
实验事实 | 数据分析及结论 |
1.8g葡萄糖完全燃烧,得到2.64gCO2和1.08gH2O | 数据___________________________ 结论:葡萄糖含有C、H、O三种元素 |
(讨论交流)为了尽量减少误差:
(1)该实验在进行过程中应注意的问题是_______________(1条)。
(2)从定量实验的角度看,该实验可进一步改进。请简要写出一个改进意见:________。
【题目】人类的生产、生活离不开水和溶液。
(1)自来水厂净水过程中使用了活性炭,这是因为活性炭具有_________作用。
(2)现有软水和硬水样品各一瓶,请设计实验对它们进行区分,并完成实验报告。
实验步骤 | 实验现象及结论 |
____ | ____ |
(3)下表是氯化钠、硝酸钾在不同温度时的溶解度。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | |
下列说法正确的是_________(填字母)。
A 氯化钠的溶解度大于硝酸钾的溶解度
B 20℃时,将30g氯化钠加入50 g水中,充分搅拌,所得溶液中溶质的质量分数为37.5%
C 分别将80℃时硝酸钾的饱和溶液和氯化钠的饱和溶液降温至30℃,析出硝酸钾晶体的质量比析出氯化钠晶体的质量大
D 从含有少量氯化钠的硝酸钾的饱和溶液中得到较多的硝酸钾晶体,通常可采用冷却热饱和溶液的方法
(4)下图是一定溶质质量分数的氯化钠溶液的配制流程。
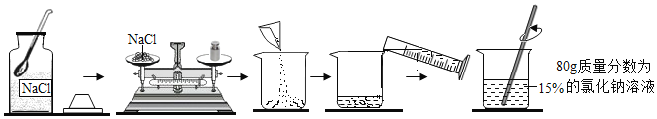
①实验步骤依次为:_________、称量、量取、溶解。用量筒量取所需的水时,若采用仰视的方法读数,配制的氯化钠溶液中溶质的质量分数会_________(填“偏大”或“偏小”)。
②将20g质量分数为6%的氯化钠溶液与30g质量分数为4%的氯化钠溶液充分混合,所得溶液中溶质的质量分数为_________。
(5)在0℃时,氮气的溶解度为0.024。这句话的含义是_______________________。