题目内容
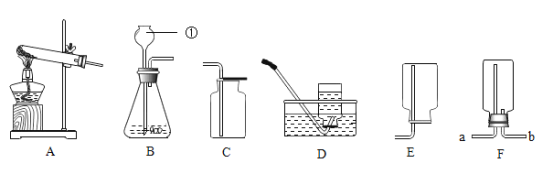
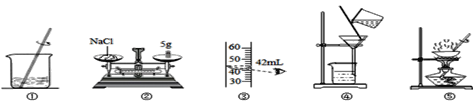
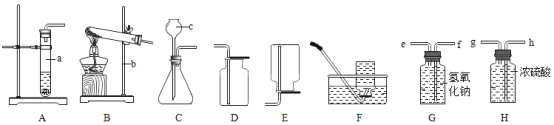
【题目】某化学兴趣小组用如图所示的装置(装置气密性良好)来制取干燥的氧气,并测定H2O2溶液中溶质的质量分数。下列说法正确的( )
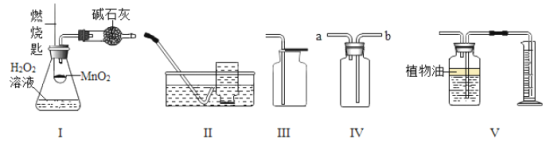
A. 将装置I分别与装置II、III、IV、V连接,均能达到实验目的
B. 称量装置I反应前及完全反应冷却后的质量,可计算出![]() 溶液中溶质的质量分数
溶液中溶质的质量分数
C. 若用装置IV收集氧气,可将带火星的木条放置在b导管口处验满
D. 若用装置V测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大
【答案】B
【解析】
A、将装置I分别与装置II、III、IV、V连接,装置II为排水法,收集的气体不干燥,选项错误;
B、称量装置I反应前及完全反应冷却后的质量,能计算出生成氧气的质量,进而可计算出H2O2溶液中溶质的质量分数正确,选项正确;
C、若用装置IV收集氧气,氧气应从b管进入瓶中,可将带火星的木条放置在a处验满,选项错误;
D、若用装置V测量生成氧气的体积,集气瓶上方原有的空气对测量结果无影响,所以不会使测量结果偏大,选项错误,故选B。

【题目】依据下列实验和数据回答下列小题。
向100 g水中加入固体A或改变温度,得到相应的溶液①~③。
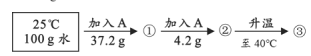
资料:A的溶解度 | |||
温度/℃ | 20 | 30 | 40 |
溶解度/g | 37.2 | 41.4 | 45.8 |
【1】在通常情况下,下列溶液中一般得不到饱和溶液的是
A. 硝酸钾溶液B. 二氧化碳溶液C. 酒精溶液D. 氯化钠溶液
【2】下列说法中,正确的是
A. 配制溶液时,搅拌可以增大固体溶质的溶解度
B. 金属与酸溶液发生置换反应后,溶液质量一定增加
C. 不饱和溶液变为饱和溶液,溶质质量分数一定变大
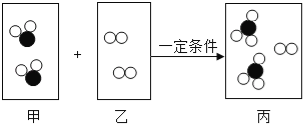
D. 有单质和化合物生成的反应一定是置换反应
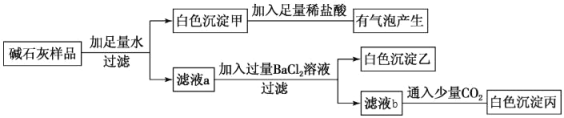
【题目】某化学学习小组在老师的指导下,对白色粉笔的成分进行探究。
(提出问题)白色粉笔的主要成分是什么呢?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
(猜想与假设)同学分别做出如下猜想:
A 碳酸钙 B 氢氧化钙 C 硫酸钙 D 氯化钙 E 硝酸钙
同学们根据老师提示并讨论,立即否定了B的猜想,你认为理由是________.
(查阅资料)
(1)硫酸钙是自然界中石膏矿的主要成分,为白色固体,微溶于水.
(2)室温下几种物质的溶解度
物质 | 碳酸钙 | 氯化钙 | 硫酸钙 | 硝酸钙 |
溶解度/g | 0.0013 | 74.5 | 0.3 | 138 |
(进行实验)
实验操作 | 现象 | 结论 | |
① | 取少量白色粉笔研碎于试管中,加入________ | 无现象 | A不成立 |
② | 取少量白色粉笔研碎于烧杯中,加入少量水,搅拌 | 固体没有明显减少 | ________不成立 |
③ | 将②进行________操作,得到清液A和固体,向清液中加入 ____________溶液,再加入足量稀盐酸 | 产生白色沉淀,沉淀不消失 | C成立 |
请写出③中发生反应的化学方程式___________.
(拓展延伸)为了测定生石膏的组成(CaSO4·xH2O),即测定x的值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下,并利用数据绘制的图象如图所示。
查阅资料:含结晶水的硫酸钙有两种组成形式,在加热过程中,分步失去结晶水,最终得到硫酸钙固体。
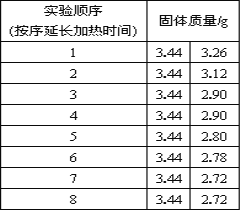

(1)AB段固体质量不变的原因__________。
(2)利用实验数据,计算x= ________.
(3)图中CD段固体物质的化学式 _____________.