题目内容
【题目】现有六种物质,O2、Fe、Fe2O3、稀H2SO4、NaOH溶液、CuSO4溶液.将它们两两混合,在常温下,一共能发生_____个反应,写出其中一个反应后溶液的质量减少的反应的化学方程式_____.
【答案】5 ![]()
【解析】
由题意在O2、Fe、Fe2O3、稀H2SO4、NaOH溶液、CuSO4溶液六种物质中:
氧气和铁可以反应,在点燃条件下生成四氧化三铁;
铁和稀硫酸可以反应生成硫酸亚铁和氢气;
铁和硫酸铜可以反应生成硫酸亚铁和铜;
氧化铁可以和硫酸反应生成硫酸铁和水;
硫酸可以和氢氧化钠反应生成硫酸钠和水;
氢氧化钠可以和硫酸铜反应生成氢氧化铜和硫酸钠;
综上所述,铁和氧气是在点燃条件下发生反应,故在常温下,一共能发生5个反应;
上述5个常温下发生的反应中:
铁和稀硫酸可以反应生成硫酸亚铁和氢气,反应后溶液的质量增加;
铁和硫酸铜反应生成硫酸亚铁和铜,参加反应的铁的质量小于生成的铜的质量,反应后溶液质量减小,反应的化学方程式为![]() ;
;
氧化铁可以和硫酸反应生成硫酸铁和水,反应后溶液的质量增加;
硫酸可以和氢氧化钠反应生成硫酸钠和水,反应前后溶液的质量不变;
氢氧化钠可以和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,生成沉淀,反应后溶液的总质量减小,反应的化学方程式为![]() 。
。

【题目】某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
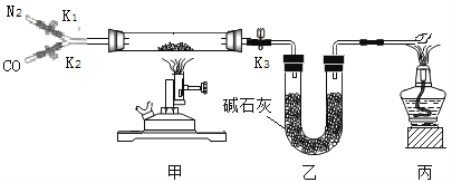
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤II硬质玻璃 管和剩余固体 | 步骤步骤Ⅲ硬质玻璃 管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2-m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3-m4