题目内容
用含杂质(杂质不与酸反应)的铁10克,与50克稀硫酸恰好完全反应,滤去杂质后,试管中的液体质量是55.4克,则含杂质的铁中铁的质量分数是
- A.28%
- B.56%
- C.54%
- D.缺少数据,无法确定
B
分析:利用一定量金属完全反应产生氢气质量=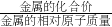 ×金属质量,铁与酸和盐发生置换反应时,铁元素的化合价应使用+2价,通过假设铁的质量,根据反应中铁与产生氢气的质量关系,利用质量守恒定律,解决所假设的铁的质量即可完成此杂质的铁中铁的质量分数的计算.
×金属质量,铁与酸和盐发生置换反应时,铁元素的化合价应使用+2价,通过假设铁的质量,根据反应中铁与产生氢气的质量关系,利用质量守恒定律,解决所假设的铁的质量即可完成此杂质的铁中铁的质量分数的计算.
解答:设铁的质量为x,则完全反应生成氢气的质量=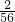 ×x,
×x,
根据质量守恒定律,x+50g=55.4g+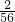 ×x,
×x,
解得x=5.6g
则此铁中铁的质量分数= ×100%=56%.
×100%=56%.
故选B.
点评:只有熟记一定量金属完全反应产生氢气质量=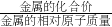 ×金属质量,才能快速解答本题,同学应对一些能简化过程、节省做题时间的公式做到熟记.
×金属质量,才能快速解答本题,同学应对一些能简化过程、节省做题时间的公式做到熟记.
分析:利用一定量金属完全反应产生氢气质量=
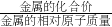 ×金属质量,铁与酸和盐发生置换反应时,铁元素的化合价应使用+2价,通过假设铁的质量,根据反应中铁与产生氢气的质量关系,利用质量守恒定律,解决所假设的铁的质量即可完成此杂质的铁中铁的质量分数的计算.
×金属质量,铁与酸和盐发生置换反应时,铁元素的化合价应使用+2价,通过假设铁的质量,根据反应中铁与产生氢气的质量关系,利用质量守恒定律,解决所假设的铁的质量即可完成此杂质的铁中铁的质量分数的计算.解答:设铁的质量为x,则完全反应生成氢气的质量=
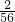 ×x,
×x,根据质量守恒定律,x+50g=55.4g+
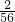 ×x,
×x,解得x=5.6g
则此铁中铁的质量分数=
 ×100%=56%.
×100%=56%.故选B.
点评:只有熟记一定量金属完全反应产生氢气质量=
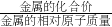 ×金属质量,才能快速解答本题,同学应对一些能简化过程、节省做题时间的公式做到熟记.
×金属质量,才能快速解答本题,同学应对一些能简化过程、节省做题时间的公式做到熟记. 
练习册系列答案
相关题目
用含杂质(杂质不与酸反应)的铁10克与50克稀硫酸充分反应,铁消耗完.滤去杂质,溶液的质量为55.4克.则此铁的纯度是( )
| A、无法确定 | B、84% | C、28% | D、56% |