题目内容
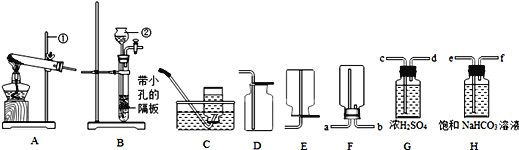
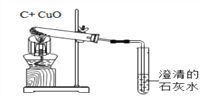
【题目】如图所示A是氧化物,可作干燥剂;已知F、K常温下为无色液体,且组成元素相同,G、L、X、E都为黑色固体,X、E为单质,G、L为氧化物。(通常情况下)B、D、H为气体,它们之间发生如图变化,请你根据所学的化学知识作出推断:
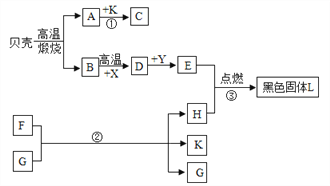
(1)反应①由A→C的过程是__________(“放出”或“吸收”)热量的;
(2)贝壳的主要成分是___________(写名称),贝壳高温煅烧的化学方程式___________;
(3)B→D的化学方程式___________________;
(4)B的固态的用途是______________;
(5)E与H生成L的现象是______________________________。
【答案】 放出 碳酸钙 CaCO3![]() CaO+CO2↑ CO2+C
CaO+CO2↑ CO2+C![]() 2CO 人工降雨(合理即可) 剧烈燃烧,放出大量的热,火星四射,生成黑色固体
2CO 人工降雨(合理即可) 剧烈燃烧,放出大量的热,火星四射,生成黑色固体
【解析】本题属于推断题,根据题目给出的流程图和信息:贝壳的主要成分是碳酸钙,碳酸钙在高温下生成氧化钙和二氧化碳,A是氧化物,可作干燥剂, A是氧化钙,B是二氧化碳;氧化钙和水生成氢氧化钙,已知F、K常温下为无色液体,且组成元素相同,则C是氢氧化钙,F是过氧化氢,K是水;二氧化碳和黑色固体单质碳在高温的条件下生成一氧化碳,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,因此X是碳,D是一氧化碳,Y是氧化铁,E是铁;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,因此G是二氧化锰,H是氧气;铁和氧气在点燃的条件下生成四氧化三铁,因此L是四氧化三铁。因此:
(1)由A→C的过程中是氧化钙和水生成氢氧化钙,是放热反应;
(2)贝壳的主要成分是碳酸钙,碳酸钙在高温下生成氧化钙和二氧化碳,反应的化学方程式是:CaCO3![]() CaO+CO2↑;
CaO+CO2↑;
(3)B→D的反应是二氧化碳和黑色固体单质碳在高温的条件下生成一氧化碳,反应的化学方程式是:CO2+C![]() 2CO;
2CO;
(4)B是二氧化碳,二氧化碳的固体叫干冰,干冰可以进行人工降雨,也可以做制冷剂等;
(5)E与H生成L的反应是铁在氧气中燃烧,现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体。

【题目】去年党的十九大会议使用了一种含碳酸钙的“石头纸”。为测定其中碳酸钙的含量,课外活动小组的同学共称取50g碎纸样品,分别放在5只烧杯中并编号,再分别向5只烧杯中加入浓度相同的稀盐酸进行实验。实验数据见下表(假设纸张中的其他成分既不溶于水,也不与盐酸反应):
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | m | 3.52 |
(1)表中m的值为___________。
(2)求样品中碳酸钙的质量分数___________。
(3)求样品中碳酸钙和盐酸刚好完全反应后得到溶液溶质的质量分数(结果保留到小数点后第二位)___